题目内容
7.用“侯氏制碱法”制得的纯碱中常含有少量的氯化钠(假定只含氯化钠杂质).某化学兴趣小组为了测定纯碱样品中碳酸钠的质量分数,做了如下实验:称量纯碱样品12g,加入到138.7g的氯化钡溶液中,恰好完全反应.过滤干燥后,称得沉淀质量为19.7g.请计算:(1)纯碱样品中碳酸钠的质量分数(计算结果精确到0.1%);
(2)所得溶液中溶质质量分数.
分析 样品中只有碳酸钠和氯化钡溶液反应生成碳酸钡沉淀,所以根据化学方程式计算出碳酸钠的质量和生成的氯化钠的质量,进而计算出碳酸钠的质量分数和所得溶液中溶质质量分数.
解答 解:(1)设碳酸钠的质量为x生成氯化钠的质量为y
Na2CO3+BaCl2═BaCO3↓+2NaCl
106 197 117
x 19.7g y
$\frac{106}{x}=\frac{197}{19.7g}=\frac{117}{y}$
x=10.6g,y=11.7g
纯碱样品中碳酸钠的质量分数:$\frac{10.6g}{12g}×100%$=88.3%;
答:纯碱样品中碳酸钠的质量分数为88.3%;
(2)所得溶液中溶质质量分数:$\frac{12g-10.6g+11.7g}{12g+138.7g-19.7g}×100%$=10%.
答:所得溶液中溶质质量分数为10%.
点评 根据化学反应方程式计算的过程中,一定要注意:(1)设未知量x时,x的后面不要带单位;(2)书写化学方程式的时候,切记严格地按照“写→配→标→注”步骤细心书写;(3)找质量关系时,最好先找下一行的实际质量关系(即已知量和未知量),然后再对应着找上一行的相对质量关系.并且,切记将它们都写在相应的化学式的正下方,分居上下两行.(4)列比例式时,要按照“上一行的相对质量比等于下一行的实际质量比”的顺序来列;保证是对应比相等.(5)求算x时,可以参考着化学方程式下面的两行质量关系中的上下或左右的倍数关系来求算.当没有倍数关系时,再按照一般的方法来求算便是.(6)在写答案时,只需要简明扼要地答出关键语句即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
18.中国药学家屠呦呦研制的抗疟药青蒿素,挽救了全球数百万人的生命,她因此荣获2015年诺贝尔医学奖.下面关于青蒿素(化学式是C15H22O5)的说法正确的是( )
| A. | 青蒿素属于无机化合物 | |
| B. | 一个青蒿素分子由42个原子构成 | |
| C. | 青蒿素中氢元素的质量分数最大 | |
| D. | 青蒿素中碳、氢、氧三种元素的质量比为15:22:5 |
12.新装修房室内存在甲醛(CH2O)、苯(C6H6)等有害物质.下列叙述错误的是( )
| A. | 甲醛和苯都属于有机物 | |
| B. | 甲醛分子中含有水分子 | |
| C. | 甲醛中碳元素质量分数为40% | |
| D. | 苯中碳元素与氢元素的质量比为12:1 |
19.下列图示实验操作中,正确的是( )
| A. | 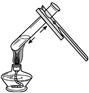 加热液体 | B. | 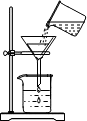 过滤 | C. | 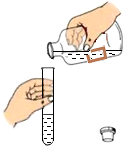 倾倒液体 | D. |  熄灭酒精灯 |
16.下列各组离子可在同一溶液中大量共存的是( )
| A. | Fe3+SO42- H+Cl- | B. | Mg2+Cl- OH- Na+ | ||
| C. | H+SO42- K+CO32- | D. | Na+Ba2+NO3 SO42- |



