题目内容
20. 取硫酸与硫酸镁的混合溶液25g放入烧杯中,逐滴滴入质量分数为5%的NaOH溶液,产生沉淀质量与滴入NaOH溶液质量的关系如图所示.
取硫酸与硫酸镁的混合溶液25g放入烧杯中,逐滴滴入质量分数为5%的NaOH溶液,产生沉淀质量与滴入NaOH溶液质量的关系如图所示.(1)与硫酸镁反应的NaOH的质量为4gg.
(2)原硫酸与硫酸镁的混合溶液中硫酸镁的质量分数(写出计算过程).
分析 向硫酸和硫酸镁的混合溶液滴加氢氧化钠溶液,硫酸、硫酸镁都可与氢氧化钠发生反应,由于硫酸的存在氢氧化钠与硫酸镁不能生成氢氧化镁沉淀,待硫酸反应完才能产生氢氧化镁沉淀;所以图象记录数据中,加入2g氢氧化钠溶液时产生沉淀的质量为0;而在加入氢氧化钠溶液6g时,产生沉淀不再增加,说明硫酸镁已完全反应,;根据硫酸镁与氢氧化钠反应的化学方程式,由氢氧化钠的质量可计算混合溶液中硫酸镁的质量从而可计算出硫酸镁的质量分数.
解答 解:(1)向硫酸和硫酸镁的混合溶液滴加氢氧化钠溶液,硫酸、硫酸镁都可与氢氧化钠发生反应,由于硫酸的存在氢氧化钠与硫酸镁不能生成氢氧化镁沉淀,待硫酸反应完才能产生氢氧化镁沉淀;由图示可知,与硫酸镁反应的NaOH的质量为(6g-2g)=4g;
设25g溶液中硫酸镁的质量为x,
MgSO4+2NaOH=Mg(OH)2↓+Na2SO4
120 80
x 4g×5%
$\frac{120}{x}=\frac{80}{4g×5%}$
x=0.3g
25g溶液中硫酸镁的质量分数=$\frac{0.3g}{25g}$×100%=1.2%.
答:溶液中硫酸镁的质量分数为1.2%.
故答案为:(1)4g;(2)1.2%.
点评 学生应熟悉利用化学方程式计算的思路和格式,能利用恰好反应及元素守恒和分析数据来解答.

练习册系列答案
 一本好题口算题卡系列答案
一本好题口算题卡系列答案
相关题目
1.用分子的观点对下列现象的解释错误的是( )
| 选项 | 现象 | 解释 |
| A | 水结成冰后体积变大 | 分子间隔变大 |
| B | 破碎的玻璃无法复原 | 分子间存在斥力 |
| C | 闻到路边怡人的花香 | 分子不停地运动 |
| D | 两块表面平滑的铅块紧压后会结合起来 | 分子间存在引力 |
| A. | A | B. | B | C. | C | D. | D |
11.如图所示的实验操作能达到实验目的是( )
| A. | 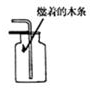 用燃着的木条检验二氧化碳 | B. |  加热蒸发食盐水 | ||
| C. | 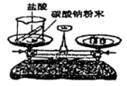 用盐酸和碳酸钠反应验证质量守恒 | D. | 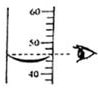 用量筒试量取46mL的水 |
12.茶叶中含有的茶氨酸(C7H14O3N2)可以降低血压,提高记忆力、保护神经细胞等,下列有关茶氨酸的说法中,正确的是( )
| A. | 茶氨酸中碳、氢元素的质量比为1:2 | |
| B. | 一个茶氨酸分子中含有1个氮分子和1个臭氧分子 | |
| C. | 茶氨酸中氢元素的质量分数最大 | |
| D. | 茶氨酸属于有机化合物 |

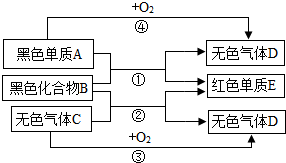 A是非金属,E是金属,B、C、D是化合物,它们之间有如图所示的转化关系(反应条件已略去):
A是非金属,E是金属,B、C、D是化合物,它们之间有如图所示的转化关系(反应条件已略去):