题目内容
9.完成下列变化的化学方程式,并按要求填空.(1)煅烧石灰石制生石灰和二氧化碳:CaO+H2O═Ca(OH)2.该反应是放热(选填“吸热”或“放热”)反应.
(2)钢铁厂用一氧化碳还原磁铁矿(主要成分四氧化三铁)炼铁:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2该反应中气体的化学计量数之比为1:1:
(3)某些工厂用稀硫酸清洗铁制品表面的铁锈(主要成分氧化铁):Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;溶液由无色变为黄色.
(4)氯化铵晶体(NH4Cl)和熟石灰混合研磨生成氯化钙和水,同时生成一种氨臭味的气体(NH3):2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑,检验该气体可用红色石蕊试纸.
分析 首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答 解:(1)石灰石高温煅烧生成生石灰和二氧化碳,反应的化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,该反应为吸热反应;
(2)四氧化三铁能被一氧化碳还原为铁,同时生成二氧化碳,化学反应方程式是:Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;反应中气体的化学计量数之比为4:4=1:1.
(3)稀硫酸和铁锈反应生成硫酸铁和水,硫酸铁溶液呈黄色,反应的化学方程式为:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O.
(4)氯化铵晶体(NH4Cl)和熟石灰混合研磨生成氯化钙和水,同时生成一种氨臭味的气体氨气,反应的化学方程式为:2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑;检验氨气可用检验该气体可用红色石蕊试纸.
故答案为::(1)CaO+H2O═Ca(OH)2;放热;
(2)Fe3O4+4CO$\frac{\underline{\;高温\;}}{\;}$3Fe+4CO2;1:1;
(3)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O;黄;
(4)2NH4Cl+Ca(OH)2═CaCl2+2H2O+2NH3↑;红色石蕊.
点评 此题主要考查化学方程式的书写,书写化学方程式时一定要遵循质量守恒定律,依据客观事实,不能臆造.

练习册系列答案
相关题目
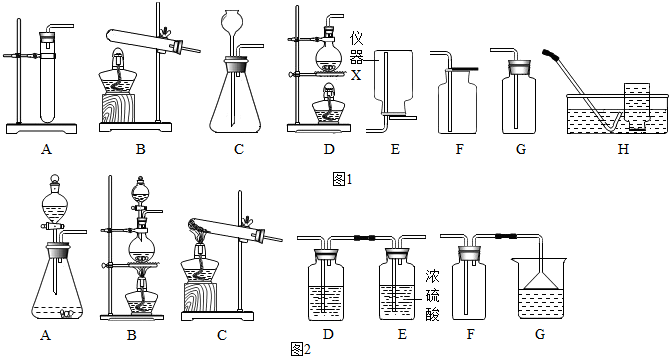
6.以下化学实验的基本操作正确的是( )
| A. | 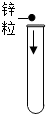 | B. | 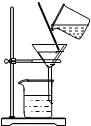 | C. | 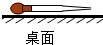 | D. | 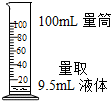 |
19.在Cu(NO3)2和AgNO3的混合溶液中,加入一定量的铁粉,充分反应后,发现有少量的金属析出,过滤后往滤液中加入盐酸无明显现象,则析出的少量金属一定含有( )
| A. | Cu | B. | Ag | C. | Cu和Ag | D. | 无法判断 |
 在一烧杯中盛有Na2CO3 和NaOH的混合物15g,向其中加入100g水,固体全部溶解.向所得溶液中滴加澄清石灰水,产生沉淀的质量与滴入石灰水的质量关系曲线如图所示.请根据题意回答下列问题:
在一烧杯中盛有Na2CO3 和NaOH的混合物15g,向其中加入100g水,固体全部溶解.向所得溶液中滴加澄清石灰水,产生沉淀的质量与滴入石灰水的质量关系曲线如图所示.请根据题意回答下列问题: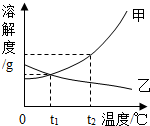 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.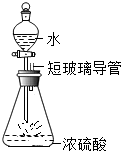 如图,在500mL锥形瓶中盛约25mL浓硫酸.将分液漏斗中的水缓慢滴人锥形瓶中.观察到的现象是水沸腾,液滴飞溅,解释产生此现象的原因是:水的密度较小,浮在浓硫酸的上面,浓硫酸溶解时放出的热会使水立刻沸腾,使液滴向四周飞溅,若堵塞短玻璃导管可能产生的后果是把瓶塞弹出或导致锥形瓶炸裂,理由是若堵塞导管,气体无法导出,膨胀的气体使瓶内气压变大,大于外界气压,把胶塞弹出或使锥形瓶炸裂.
如图,在500mL锥形瓶中盛约25mL浓硫酸.将分液漏斗中的水缓慢滴人锥形瓶中.观察到的现象是水沸腾,液滴飞溅,解释产生此现象的原因是:水的密度较小,浮在浓硫酸的上面,浓硫酸溶解时放出的热会使水立刻沸腾,使液滴向四周飞溅,若堵塞短玻璃导管可能产生的后果是把瓶塞弹出或导致锥形瓶炸裂,理由是若堵塞导管,气体无法导出,膨胀的气体使瓶内气压变大,大于外界气压,把胶塞弹出或使锥形瓶炸裂.