题目内容
1.某科学兴趣小组为验证Ag、Fe、Cu三种金属的活动性顺序,设计了如图所示的实验操作.其中可以达到实验目的组合是( )
| A. | ①③ | B. | ②③ | C. | ④⑤ | D. | ②④ |
分析 在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来;可根据“反应则活泼,不反应则不活泼”进行分析判断,通过分析方案所能得到的结论,确定是否能得出Ag、Fe、Cu三种金属的活动性顺序,判断可以达到实验目的组合.
解答 解:A、①中铁能与硫酸铜反应,说明铁的金属活动性比铜强,即Fe>Cu;③中铜不能与硫酸亚铁溶液反应,说明铜的金属活动性比铁弱,即Fe>Cu;该组合无法得出Ag、Cu两种金属的活动性顺序,故选项错误.
B、②中铜能与硝酸银溶液反应,说明铜的金属活动性比银强,即Cu>Ag;③中铜不能与硫酸亚铁溶液反应,说明铜的金属活动性比铁弱,即Fe>Cu;该组合能得出Ag、Fe、Cu三种金属的活动性顺序为Fe>Cu>Ag,故选项正确.
C、④中铁能与稀盐酸反应,说明铁的金属活动性比氢强,即Fe>H;⑤中银不能与稀盐酸反应,说明银的金属活动性比氢弱,即H>银;该组合无法得出Fe、Cu两种金属的活动性顺序,故选项错误.
D、②中铜能与硝酸银溶液反应,说明铜的金属活动性比银强,即Cu>Ag;④中铁能与稀盐酸反应,说明铁的金属活动性比氢强,即Fe>H;该组合无法得出Fe、Cu两种金属的活动性顺序,故选项错误.
故选:B.
点评 本题难度不大,考查金属活动性应用,掌握金属活动性应用“反应则活泼、不反应则不活泼”是正确解答此类题的关键.

练习册系列答案
相关题目
11.如图各项实验操作正确的是( )
| A. | 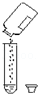 液体药品取用 | B. | 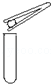 向试管中添加块状固体 | ||
| C. |  取用粉末状药品 | D. | 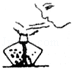 熄灭酒精灯 |
12.有一包白色粉末可能由CaCO3、Na2CO3、Na2SO4、BaCl2、NaCl中的一种或几种组成.把少量该粉末放入足量水中,搅拌、静置、过滤,得到白色固体和滤液.向所得固体中加入稀硝酸,固体溶解并有气体放出.向所得溶液中加入稀硫酸,有白色固体生成.该粉末中肯定没有的物质是( )
| A. | CaCO3 | B. | Na2SO4 | C. | BaCl2 | D. | Na2CO3 |
9. 在学习过程中,小雨同学提出一个问题:“碳燃烧时可能生成CO2,也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?”
在学习过程中,小雨同学提出一个问题:“碳燃烧时可能生成CO2,也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?”
【猜想】碳与氧化铜反应生成的气体中:
①CO ②CO2 ③CO和CO2.
【设计方案】实验前后分别对试管和烧杯里的物质进行称量,
数据设计如下:
(1)若△m2=0,说明反应产生的气体不被澄清石灰水吸收,则猜想①成立.
(2)若猜想②正确,理论上△m1与△m2 的关系是:△m1=△m2(填“>”、“<”或“=”)
【实验并记录】实验得到的数据如下表:
用以上实验数据分析,结果应该是猜想③成立.
【反思与评价】经查阅资料知道:木炭还原氧化铜时是产生CO2气体,即反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.本次实验结果与资料结果不一致.对其可能原因下列分析中合理的是ABCD
A.生成的CO2部分与过量的C反应生成了CO B.装置漏气
C.澄清石灰水吸收CO2效果不好 D.装置内还有CO2气体未被吸收.
 在学习过程中,小雨同学提出一个问题:“碳燃烧时可能生成CO2,也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?”
在学习过程中,小雨同学提出一个问题:“碳燃烧时可能生成CO2,也可能生成CO,那么碳与氧化铜反应生成的气体是否也有多种可能?”【猜想】碳与氧化铜反应生成的气体中:
①CO ②CO2 ③CO和CO2.
【设计方案】实验前后分别对试管和烧杯里的物质进行称量,
数据设计如下:
| 称量对象 | 反应前质量 | 反应后质量 | 质量差 |
| 试管+固体混合物 | M1 | M2 | △m1即( M1-M2) |
| 烧杯+澄清石灰水 | M3 | M4 | △m2即( M4-M3) |
(2)若猜想②正确,理论上△m1与△m2 的关系是:△m1=△m2(填“>”、“<”或“=”)
【实验并记录】实验得到的数据如下表:
| 称量对象 | 反应前质量 | 反应后质量 | 质量差 |
| 试管+固体混合物 | 69.8g | 65.4g | △m1 |
| 烧杯+澄清石灰水 | 118.8g | 122.6g | △m2 |
【反思与评价】经查阅资料知道:木炭还原氧化铜时是产生CO2气体,即反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑.本次实验结果与资料结果不一致.对其可能原因下列分析中合理的是ABCD
A.生成的CO2部分与过量的C反应生成了CO B.装置漏气
C.澄清石灰水吸收CO2效果不好 D.装置内还有CO2气体未被吸收.
6. 2014年3月22日是第二十二届“世界水日”.本届“世界水日”的宣传主题是“水与能源”.下列有关水说法正确的是( )
2014年3月22日是第二十二届“世界水日”.本届“世界水日”的宣传主题是“水与能源”.下列有关水说法正确的是( )
 2014年3月22日是第二十二届“世界水日”.本届“世界水日”的宣传主题是“水与能源”.下列有关水说法正确的是( )
2014年3月22日是第二十二届“世界水日”.本届“世界水日”的宣传主题是“水与能源”.下列有关水说法正确的是( )| A. | 水由氢、氧两种元素组成,故水是混合物 | |
| B. | pH=0的水溶液,是中性的溶液 | |
| C. | 从水中可获得新能源--氢能源 | |
| D. | 水是一种万能溶剂 |
13. 下表是a、b、c三种物质在不同温度时的溶解度,请根据表中数据回答:
下表是a、b、c三种物质在不同温度时的溶解度,请根据表中数据回答:
(1)从0℃升温到60℃,等量的水中能溶解的质量变化最大的物质是a(选填“a”、“b”或“c”).
(2)如图所示,现有20℃时等质量的a、b两物质的饱和溶液,试管底部有等质量的a、b剩余,向烧杯的水中加入氢氧化钠固体,则对相关变化判断正确的有C.(析出的固体中不含水,不考虑溶剂的蒸发)
A.b溶液将由饱和变成不饱和
B.a溶液中溶剂质量等于b溶液中溶剂质量
C.变化后a溶液的溶质质量分数大于b溶液的溶质质量分数.
 下表是a、b、c三种物质在不同温度时的溶解度,请根据表中数据回答:
下表是a、b、c三种物质在不同温度时的溶解度,请根据表中数据回答:| 温度/℃ | 0 | 20 | 30 | 40 | 60 | |
| 溶解度/g | 物质a | 13.3 | 31.6 | 45.8 | 63.9 | 110 |
| 物质b | 21.4 | 9.84 | 7.24 | 5.63 | 3.87 | |
| 物质c | 11.9 | 21.7 | 28.4 | 36.6 | 59.2 | |
(2)如图所示,现有20℃时等质量的a、b两物质的饱和溶液,试管底部有等质量的a、b剩余,向烧杯的水中加入氢氧化钠固体,则对相关变化判断正确的有C.(析出的固体中不含水,不考虑溶剂的蒸发)
A.b溶液将由饱和变成不饱和
B.a溶液中溶剂质量等于b溶液中溶剂质量
C.变化后a溶液的溶质质量分数大于b溶液的溶质质量分数.
10.氢气和氧气的混合气体共5克,点燃,使它们充分反应后恢复到常温,生成4.5克的水.关于原混合气体的说法中正确的是( )
①可能是2.5克氢气和2.5克氧气 ②可能是1克氢气和4克氧气
③可能是0.5克氢气和4.5克氧气 ④可能是0.5克氢气和4克氧气.
①可能是2.5克氢气和2.5克氧气 ②可能是1克氢气和4克氧气
③可能是0.5克氢气和4.5克氧气 ④可能是0.5克氢气和4克氧气.
| A. | 只有①正确 | B. | 只有②③正确 | C. | ①②③都正确 | D. | 只有④正确 |
11.德国化学家格哈德•埃特尔在固体表面化学的研究中取得了非凡的成就,其成果之一是揭示了氦气与氢气在催化剂表面合成氨的反应微观变化过程如图, 表示氮原子
表示氮原子 表示氢原子.下列叙述正确的是( )
表示氢原子.下列叙述正确的是( )

 表示氮原子
表示氮原子 表示氢原子.下列叙述正确的是( )
表示氢原子.下列叙述正确的是( )
| A. | 此反应有化合物参加 | |
| B. | 分子在化学变化中是可分的 | |
| C. | 符合上述反应过程的顺序是①③② | |
| D. | 对应化学反应方程式为N2+3H2$\frac{\underline{\;催化剂\;}}{\;}$2NH3 |
