题目内容
8.下列有关实验现象或事实叙述错误的是( )| A. | 切完西瓜的菜刀洗净擦干放在通风干燥处可以防止生锈 | |
| B. | 光亮的铜丝放入稀硫酸中有气泡产生 | |
| C. | 铁丝在氧气中燃烧,火星四射,生成黑色固体 | |
| D. | 铝丝在硫酸铜溶液中能形成“铜树” |
分析 A、根据铁的锈蚀条件进行分析;
B、根据铜的金属活动性排在氢的后面进行分析;
C、根据铁丝在氧气中燃烧的现象进行分析;
D、根据铝的金属活动性比铜强进行分析.
解答 解:A、铁生锈的条件是与水、氧气同时接触,所以切完西瓜后将菜刀洗净擦干放在干燥的地方,不容易生锈,故A正确;
B、铜的金属活动性排在氢的后面,铜不会与稀硫酸反应生成氢气,故B错误;
C、铁丝在氧气中燃烧,火星四射,生成黑色固体,故C正确;
D、铝的金属活动性比铜强,所以铝丝在硫酸铜溶液中能形成“铜树”,故D正确.
故选:B.
点评 本题主要考查物质的性质和用途,解答时要充分理解各种物质的性质,然后再根据物质的性质方面进行分析、判断,从而确定物质的用途.

练习册系列答案
相关题目
1.下列物质之间的转化,能通过一步反应实现的是( )
①Zn→ZnSO4
②CaO→Ca(OH)2
③H2O2→H2O
④Fe→Fe2 (SO4)3
⑤Fe3O4→Fe.
①Zn→ZnSO4
②CaO→Ca(OH)2
③H2O2→H2O
④Fe→Fe2 (SO4)3
⑤Fe3O4→Fe.
| A. | ①②③④ | B. | ①②③⑤ | C. | ①③④⑤ | D. | ②③④⑤ |
19. 黄铜是铜和锌的合金,取一定质量的黄铜样品放入烧杯中,缓慢滴加足量盐酸溶液,合金与盐酸溶液反应情况如图【提示:铜不与稀盐酸溶液反应,锌与盐酸反应的化学方程式为Zn+2HCl═ZnCl2+H2↑】,实验数据如下表:
黄铜是铜和锌的合金,取一定质量的黄铜样品放入烧杯中,缓慢滴加足量盐酸溶液,合金与盐酸溶液反应情况如图【提示:铜不与稀盐酸溶液反应,锌与盐酸反应的化学方程式为Zn+2HCl═ZnCl2+H2↑】,实验数据如下表:
求:
(1)生成氢气的质量M为0.1克.
(2)所用盐酸溶液的溶质质量分数为多少?
 黄铜是铜和锌的合金,取一定质量的黄铜样品放入烧杯中,缓慢滴加足量盐酸溶液,合金与盐酸溶液反应情况如图【提示:铜不与稀盐酸溶液反应,锌与盐酸反应的化学方程式为Zn+2HCl═ZnCl2+H2↑】,实验数据如下表:
黄铜是铜和锌的合金,取一定质量的黄铜样品放入烧杯中,缓慢滴加足量盐酸溶液,合金与盐酸溶液反应情况如图【提示:铜不与稀盐酸溶液反应,锌与盐酸反应的化学方程式为Zn+2HCl═ZnCl2+H2↑】,实验数据如下表:| 反应前 | 反 应 后 | ||
| 实验 数据 | 盐酸溶液 的质量 | 烧杯和黄铜样品 的质量 | 烧杯和剩余物 的质量 |
| 50.0g | 63.0g | 112.9g | |
(1)生成氢气的质量M为0.1克.
(2)所用盐酸溶液的溶质质量分数为多少?
13.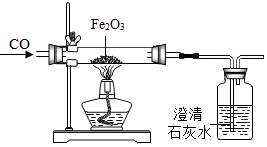 如图是一氧化碳还原氧化铁的实验.下列有关该实验的说法不正确的是( )
如图是一氧化碳还原氧化铁的实验.下列有关该实验的说法不正确的是( )
 如图是一氧化碳还原氧化铁的实验.下列有关该实验的说法不正确的是( )
如图是一氧化碳还原氧化铁的实验.下列有关该实验的说法不正确的是( )| A. | 该装置缺少尾气处理装置,会污染空气 | |
| B. | 点燃酒精灯前应持续通入CO防止发生爆炸 | |
| C. | 改用二氧化碳进行该实验也能看到完全相同的现象 | |
| D. | 利用反应前后固体质量之差能算出参加反应的一氧化碳的质量 |
 生铁是铁的合金,化学兴趣小组的同学为测定某生铁样品中铁的质量分数.进行如下实验:称取生铁样品5.8g放入烧杯中,逐滴加入稀硫酸,所加稀硫酸的质量与放出气体的质量关系如图所示(生铁样品中的杂质不与稀硫酸反应,也不溶于水).回答下列问题:
生铁是铁的合金,化学兴趣小组的同学为测定某生铁样品中铁的质量分数.进行如下实验:称取生铁样品5.8g放入烧杯中,逐滴加入稀硫酸,所加稀硫酸的质量与放出气体的质量关系如图所示(生铁样品中的杂质不与稀硫酸反应,也不溶于水).回答下列问题:
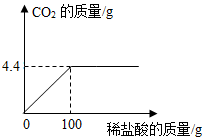 某化学兴趣小组欲测定碳酸钙样品的纯度(杂质不与盐酸反应)取12.5g样品加入到稀盐酸中,产生CO2的质量与稀盐酸的质量关系如图所示,请回答:
某化学兴趣小组欲测定碳酸钙样品的纯度(杂质不与盐酸反应)取12.5g样品加入到稀盐酸中,产生CO2的质量与稀盐酸的质量关系如图所示,请回答: