题目内容
【题目】某科学探究小组的同学取来一小块生铁(表面有铝粉涂层)片,用砂纸打磨除净涂层。为测定此样品中铁的质量分数,他们将样品放入烧杯中,再加入“足量”的稀盐酸,称量数据见下表:
除净涂层后的生铁样品质量 /g | 12 |
烧杯的质量 /g | 32.5 |
加入稀盐酸的质量 /g | 200 |
反应后烧杯及所盛物质的总质量 /g | 244.1 |
请回答下列问题:
(1)在实验中如何确保所加入的稀盐酸为“足量”?_____。
(2)计算该生铁样品中铁的质量分数_____(写出计算步骤,计算结果精确到0.1%)。
(3)按以上测定方法,则以下操作中会使该样品中铁的质量分数测定值偏小的是_____。
A 加入的稀盐酸不足量
B 换用溶质质量分数更高的盐酸进行实验
C 未将样品表面涂层(已完全氧化)打磨干净
D 将表面涂层打磨干净的生铁样品磨成粉末
【答案】继续滴加稀盐酸,观察到不再产生气泡为止 93.3% AC
【解析】
解:
(1)由于铁需要完全反应,所以加入盐酸至气体不再生成就是盐酸过量。所以足量的标准是继续滴加稀盐酸,观察到不再产生气泡为止
(2)设铁的质量为x
根据质量守恒定律,生成氢气的质量为(12+32.5+200)-244.1=0.4g
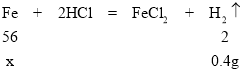
![]()
x=11.2g
该生铁样品中铁的质量分数=![]() ×100%≈93.3%
×100%≈93.3%
(3)A、加入的稀盐酸不足量,导致生成的气体少于实际值,导致结果偏小;
B、换用溶质质量分数更高的盐酸进行实验,由于盐酸具有挥发性,导致氢气质量偏大,结果偏大;
C、未将样品表面涂层(已完全氧化)打磨干净,导致铁不能完全反应,气体偏少,结果偏小;
D、将表面涂层打磨干净的生铁样品磨成粉末,使反应充分,结果准确,质量没有变化。
故选:AC。

练习册系列答案
 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案
相关题目