题目内容
11.牙膏摩擦剂的类型很多,如CaCO3,SiO2或它们的混合物.某兴趣小组对牙膏摩擦剂的成分进行了如下探究.【提出问题1】某品牌牙膏中是否含有CaCO3?
【查阅资料】二氧化硅不与稀盐酸反应.
【实验方案】①取少量牙膏于试管中,加入适量的稀盐酸,出现气泡,将气体通入澄清石灰水,石灰水变浑浊,证明摩擦剂中含有CO32-(填阴离子符号) ②取实验①中的溶液,加入碳酸钾溶液,生成白色沉淀,请写出该反应的化学方程式K2CO3+CaCl2=CaCO3↓+2KCl.
【提出问题2】该牙膏中CaCO3的质量分数是多少?
【实验装置】

【实验步骤】
(1)按如图连接好装置后,发现一处明显的错误,改正为C中导管应“长进短出”;
(2)重新连接好装置,并检查装置的气密性;
(3)在B装置中加入牙膏样品8.00g;
(4)关闭K1,打开K2,向牙膏样品中滴入10%的盐酸,至B中无气泡产生时,停止滴加
盐酸;
(5)打开K1(填“打开”或“关闭”)、并关闭K2,缓缓通入空气; 至C中不再产生沉淀;
(6)将C装置中的固液混合物过滤、洗涤、烘干后称量其质量.
实验数据如图2(已知此品牌牙膏中的其他成分不和盐酸反应,装置内试剂均足量.)

【实验分析及数据处理】
(1)若没有A装置,则测定结果将偏大.(填“偏大”、“偏小”或“不变”)
(2)D装置的作用是吸收空气中的二氧化碳干扰,防止干扰实验测定.
(3)据上面数据,计算该牙膏样品中碳酸钙的质量分数是25%.
( CO2+Ba(OH)2═BaCO3↓+H2O)
分析 【实验方案】依据碳酸根离子的检验方法分析解答,并据反应原理书写方程式;
【实验步骤】(1)洗气装置中导管应长进短出;
(2)实验前应检查装置的气密性,防止装置漏气;
(4)依据装置设计原理和实验目的分析解答;
(5)再次打开K1,关闭K2,缓缓通入一段时间空气,使生成的二氧化碳充分反应;
【实验分析及数据处理】
(1)A装置的作用是吸收空气中的二氧化碳,防止测量结果不准确;
(2)D装置的作用是吸收空气中的二氧化碳,防止测量结果不准确;
(3)依据所测生成沉淀数据的平均值,计算反应的二氧化碳的质量,并进而计算参加反应的碳酸钙的质量.
解答 解:【实验方案】①取少量牙膏于试管中,加入过量稀盐酸,出现气泡,将气体通入澄清石灰水中,石灰水变浑浊,说明生成二氧化碳,从而证明摩擦剂中含有碳酸根离子;
②实验①中的溶液中含有氯离子,加入碳酸钾溶液,生成白色沉淀-碳酸钙,说明该溶液中含有钙离子,反应的化学方程式是K2CO3+CaCl2=CaCO3↓+2KCl;
【实验步骤】(1)C的作用是吸收反应生成的二氧化碳,装置中导管应长进短出;
(2)实验前应检查装置的气密性,防止装置漏气;
(4)关闭K1,打开K2,向牙膏样品中滴入10%的盐酸,至不再生成气体,停止滴加盐酸;
(5)再次打开K1,关闭K2,缓缓通入一段时间空气,使生成的二氧化碳全部排出,充分反应,至C中不再产生沉淀;
【实验分析及数据处理】
(1)A装置的作用是吸收空气中的二氧化碳,若没有该装置,则进入C的气体还有空气中的二氧化碳,使测量结果偏大;
(2)D装置的作用是吸收空气中的二氧化碳,防止空气中二氧化碳进入,使测量结果不准确;
(3)依据所测生成沉淀数据,计算反应的二氧化碳的质量,并进而计算牙膏中碳酸钙的质量,计算过程如下;
解:根据数据得生成沉淀为3.94g,设参加反应的二氧化碳的质量为x
Ba(OH)2+CO2═BaCO3↓+H2O
44 197
x 3.94g
$\frac{44}{x}=\frac{197}{3.94g}$
x=0.88g
设碳酸钙的质量为y
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
y 0.88g
$\frac{100}{y}=\frac{44}{0.88g}$
y=2g
该牙膏样品中碳酸钙的质量分数=$\frac{2g}{8g}$×100%=25%.
故答案为:【实验方案】①CO32-;②K2CO3+CaCl2=CaCO3↓+2KCl;
【实验步骤】(1)C中导管应“长进短出”;
(2)检查装置的气密性;
(5)打开K1,关闭K2;
【实验分析及数据处理】
(1)偏大;(2)吸收空气中的二氧化碳干扰,防止干扰实验测定;(3)25%.
点评 本题难度较大,属于盐的性质中实验方法和过程的探究,根据物质的化学性质,要认真分析,不仅要把握实验设计的每一个步骤中的实验目的,装置的用途等知识,还要对有关的计算准确,能考查学生综合分析、解决问题的能力,计算牙膏中碳酸钙的含量时,也可利用关系式法求解.

 阅读快车系列答案
阅读快车系列答案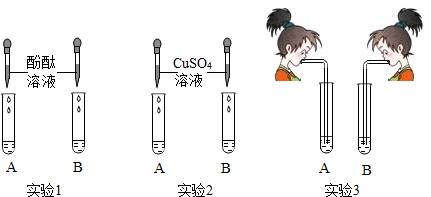
(1)实验l 中,两支试管的溶液都变成红色.
(2)实验2中,若B 盛装的是NaOH 溶液,发生反应的化学方程式为:2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
(3)实验3中,李红同学向两支试管吹气,A 中有白色沉淀生成,发生反应的化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
B 中无现象,为了探究吹气后B 中溶质的成分,李红进行了如下探究.
【提出猜想】:
猜想1:溶质只有氢氧化钠
猜想2:溶质只有碳酸钠
猜想3:溶质有氢氧化钠和碳酸钠.
【实验和结论】:
| 实验 | 实验现象 | 结论 |
| 取B 中少量溶液,加人澄清石灰水至不再 产生沉淀为止,过滤后取上层清液, 向其中加几滴酚酞试液. | 产生白色沉淀 溶液呈现红色 | 猜想3成立 |
同学们相互讨论后,李红得出的结论不正确(填“正确”或“不正确”),其原因是猜想2(填数字)也会产生相同的现象.
 某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.
某化学兴趣小组对一包干燥的红色粉末组成进行探究,该红色粉末可能由Cu、Fe2O3两种固体中的一种或两种组成.【提出猜想】红色粉末可能是:①Cu ②Fe2O3 ③Cu和Fe2O3
【查阅资料】(1)白色无水CuSO4遇水变蓝
(2)Cu在FeCl3溶液中发生反应:2FeCl3+Cu═2FeCl2+CuCl2
【实验探究】
[甲组同学]:定性检测该红色粉末的物质组成
(1)小云取少量红色粉末于试管中,滴加足量稀盐酸,充分振荡后观察,发现固体全部溶解,得有色溶液.则猜想猜想①一定不成立一定不成立,其中一定发生反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O.
(2)小伟向小云得到的有色溶液中插入一根洁净的铁丝,反应充分后,观察到铁丝表面有红色物质生成
现象,得出猜想③成立.
[乙组同学]:定量测定该红色粉末中氧化铁的质量分数
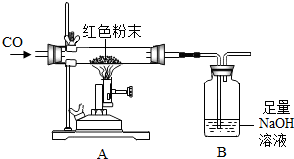
实验步骤:小晨称取该红色粉末5.0g装入硬质玻璃管中,按如图进行实验.开始时缓缓通入CO气体,过一段时间后再高温加热使其充分反应.待反应完全后,停止加热,仍继续通CO气体直至玻璃管冷却.反应前后称量相关物质的总质量(装置内空气中的水蒸气、CO2忽略不计),其数据如下表:
| 反应前 | 反应后 | |
| Ⅰ 组 | 玻璃管和红色粉末的总质量为48.3g | 玻璃管和固体物质的总质量为47.1g |
| Ⅱ 组 | 洗气瓶和瓶中所盛物质的总质量为258.6g | 洗气瓶和瓶中所盛物质的总质量为261.91g |
(1)在装置A中先通CO气体的目的是排尽玻璃管内的空气.A装置中发生反应的化学方程式为3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)根据上述表格中的实验数据计算:红色粉末中氧化铁的质量分数为80%.
(3)从环保角度看上述装置有严重不足之处.你认为应该如何改进?缺少尾气处理装置;可以在导管口放点燃酒精灯,将一氧化碳烧掉.
【拓展延伸】对实验后B装置洗气瓶内溶液中是否有NaOH 剩余做进一步探究
实验步骤:小渊同学取该洗气瓶内溶液50克,逐滴加入质量分数为7.3%的稀盐酸至无气泡冒出为止,共用去稀盐酸60克,所得溶液质量为107.8克.试通过计算说明实验后B装置洗气瓶内溶液中是否有NaOH?(写出计算过程).
【提出问题】这瓶氢氧化钠固体是否变质?
【猜想与假设】
①氢氧化钠没有变质;②该氢氧化钠部分变质;③该氢氧化钠全部变质.
【设计实验】取氢氧化钠固体样品溶于水配成溶液A,进行如下实验:
| 实验步骤 | 实验现象 | 结论及解释 |
| (1)取少量溶液A于试管中,向其中滴加足量的稀盐酸; | 有气泡产生 | 猜想①不成立 |
| (2)另取少量溶液A于试管中,向其中滴加足量的氯化钙溶液; | 产生白色沉淀 | 反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl |
| (3)将步骤(2)所得的混合液静置,向上层清液中滴加无色的酚酞溶液. | 溶液呈红色 | 猜想②成立 |
(4)久置的氢氧化钠变质的原因是(用化学方程式表示)CO2+2NaOH=Na2CO3+H2O.
【探索与拓展】为进一步探究氢氧化钠的变质程度,小明称取18.6g氢氧化钠固体样品放入烧杯中,向其中逐滴加入稀盐酸,到不再产生气泡为止,共消耗稀盐酸100g,反应后称得烧杯中溶液的质量为114.2g.
(5)求该样品中碳酸钠的质量(要写出计算过程);
(6)该氢氧化钠的变质程度(即变质的氢氧化钠占变质前的氢氧化钠的质量分数)为50%.
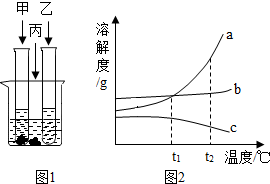 在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如图1所示,甲、丙还有剩余固体,乙固体全部溶解.升温到80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化.
在室温下,甲、乙、丙三种固体分别溶于两支试管和一个烧杯的水中,现象如图1所示,甲、丙还有剩余固体,乙固体全部溶解.升温到80℃时,发现甲固体全部溶解,乙固体析出,丙固体没有明显变化.