题目内容
2. 化学是在原子、分子、离子水平上研究物质及其变化的科学.
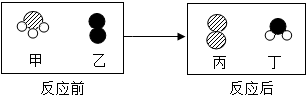
化学是在原子、分子、离子水平上研究物质及其变化的科学.(1)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如图.该反应的前后总共有3种原子.该反应是(填“是”或“不是”)置换反应.反应前后元素的化合价有(填“有”或“无”)变化.在该反应中甲和丁两种分子的个数比为2:3.
(2)胃酸过多须服用抗酸药.如表为两种抗酸药的有效成分及其构成微观粒子:
| 抗胃酸药 | 复方氢氧化镁片剂 | 铝碳酸镁片 |
| 有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
| 构成微粒 | Mg2+、OH- | Al3+、Mg2+、OH-、CO32- |
①Mg(OH)2起抗酸作用的粒子是OH-(填粒子符号,下同);
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑
则铝碳酸镁起抗酸作用的两种粒子是OH-、CO32-.
分析 (1)首先要对模型图进行观察,分析物质的微观构成、物质的类别,再找出物质之间的微粒数目关系,然后再对题中各问加以分析解答;
(2)根据酸碱中和反应、氢离子与碳酸根离子反应等方面进行分析.
解答 解:(1)根据图示可以看出,该反应的前后总共有 3种原子.该反应是一种单质和一种化合物生成一种单质和化合物,属于置换反应,反应前后,氧、氮元素的化合价均发生了改变,该反应的化学方程式为:4NH3+3O2$\frac{\underline{\;点燃\;}}{\;}$2N2+6H2O;该反应中甲和丁两种分子的个数比为2:3;
(2)胃酸的主要成分为盐酸,①Mg(OH)2中氢氧根离子能与胃酸中的盐酸中的氢离子发生中和反应生成水,从而起到中和胃酸的作用.
②AlMg(OH)3CO3中的OH-、CO32-都能中和胃酸中的氢离子.
故答案为:(1)3;是;有; 2:3;
(2)①OH-;②OH-、CO32-.
点评 本题综合性较强,但由于问题较多,容易被弄糊涂了,因此要从概念的科学定义出发,逐一解答.不能光看图示,否则容易出错.

练习册系列答案
相关题目
3.下列叙述,不正确的是( )
| A. | 乙醇属于可再生能源 | |
| B. | “可燃冰”将成为未来的新能源 | |
| C. | 将煤碳加工成蜂窝煤,能使煤燃烧更充分 | |
| D. | 化学电池是将化学能传化为热能的一种方式 |
11.“超临界水”因具有许多优良特质而被科学家追捧,它是指当气压和温度达到一定值时,水的液态和气态完全交融在一起的液体.下面有关“超临界水”的说法正确的是( )
| A. | 它是混合物 | |
| B. | 它的分子之间有间隔 | |
| C. | 它的化学性质与水不同 | |
| D. | 它的一个分子由4个氢原子和2个氧原子构成 |
12.下列各组物质的鉴别中,所选的鉴别试剂,不正确的是( )
| 选项 | 待鉴别物质 | 鉴别试剂 |
| A | 氢氧化钠溶液和氢氧化钙溶液 | 二氧化碳气体 |
| B | 鉴别硫酸铵和硫酸钠固体 | 氢氧化钡溶液 |
| C | 食盐溶液和稀盐酸 | 紫色石蕊 |
| D | 氮气和二氧化碳气体 | 燃着的木条 |
| A. | A | B. | B | C. | C | D. | D |
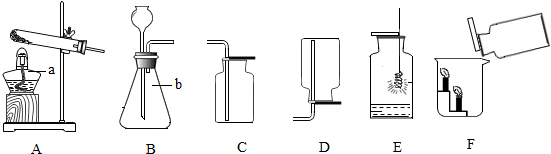
 化学兴趣小组欲用如图某胃药标签进行物质成分分析.取20片该药片研碎放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(药品中其他成分不溶于水,也不参加反应),共消耗稀盐酸25g,待反应生成的气体全部逸出,测得烧杯内物质的总质量为30.6g.
化学兴趣小组欲用如图某胃药标签进行物质成分分析.取20片该药片研碎放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(药品中其他成分不溶于水,也不参加反应),共消耗稀盐酸25g,待反应生成的气体全部逸出,测得烧杯内物质的总质量为30.6g.
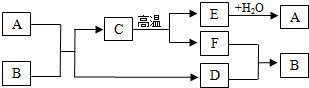 已知A、B、C、D、E、F六种物质之间存在如图所示的关系.其中A常用来改良酸性土壤,B是常见的盐,其水溶液显碱性,C是大理石的主要成分.(图中“-”表示两端的物质能反应,“→”表示物质间存在转化关系,部分物质和反应条件未标出).请按要求回答下列问题:
已知A、B、C、D、E、F六种物质之间存在如图所示的关系.其中A常用来改良酸性土壤,B是常见的盐,其水溶液显碱性,C是大理石的主要成分.(图中“-”表示两端的物质能反应,“→”表示物质间存在转化关系,部分物质和反应条件未标出).请按要求回答下列问题: