题目内容
17. 化学兴趣小组欲用如图某胃药标签进行物质成分分析.取20片该药片研碎放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(药品中其他成分不溶于水,也不参加反应),共消耗稀盐酸25g,待反应生成的气体全部逸出,测得烧杯内物质的总质量为30.6g.
化学兴趣小组欲用如图某胃药标签进行物质成分分析.取20片该药片研碎放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(药品中其他成分不溶于水,也不参加反应),共消耗稀盐酸25g,待反应生成的气体全部逸出,测得烧杯内物质的总质量为30.6g.请计算:
(1)药品中碳酸氢钠的质量分数;
(2)反应后所得溶液中溶质的质量分数.(计算结果精确是0.1%)
分析 (1)根据每片药品重0.5g计算出20片的质量;根据烧杯内质量的减少量就是二氧化碳的质量;根据二氧化碳的质量计算出碳酸氢钠的质量,再除以药品的质量即可;
(2)根据二氧化碳的质量算出反应后生成的溶质质量,再除以反应后所得溶液的质量即可.
解答 解:每片药品重0.5g,所以20片药品的质量为0.5g×20=10g;反应共生成气体的质量为10g+25g-30.6g=4.4g;
设要生成4.4g二氧化碳需要参加反应的碳酸氢钠质量为x,生成氯化钠质量为y则:
NaHCO3+HCl═NaCl+H2O+CO2↑
84 58.5 44
x y 4.4g
$\frac{84}{x}=\frac{58.5}{y}=\frac{44}{4.4g}$
x=8.4g
y=5.85g
(1)药品中碳酸氢钠的质量分数=$\frac{8.4g}{10g}×$100%=8.4%;
(2)反应后所得溶液质量为:8.4g+25g-4.4g=29g.
反应后所得溶液中溶质的质量分数:$\frac{5.85g}{29g}×$100%=20.2%
答案:
(1)药品中碳酸氢钠的质量分数为8.4%;
(2)反应后所得溶液中溶质的质量分数为20.2%.
点评 本题容易出错的地方是反应后所得溶液的计算,杂质不能加入,只能加碳酸氢钠和盐酸质量,再减去气体的质量.

练习册系列答案
相关题目
19.下列实验不能取得预期效果的是( )
| A. | 用酚酞试液区别稀硫酸与食盐水 | |
| B. | 用水区别氢氧化钠和硝酸铵固体 | |
| C. | 用灼烧闻气味的方法区别羊毛和涤纶 | |
| D. | 用相互刻划法比较黄铜片和纯铜片硬度的大小 |
12.把少量的下列物质分别放入水中,充分搅拌后,可以得到溶液的是( )
| A. | 面粉 | B. | 胆矾 | C. | 沙土 | D. | 汽油 |
2. 化学是在原子、分子、离子水平上研究物质及其变化的科学.
化学是在原子、分子、离子水平上研究物质及其变化的科学.
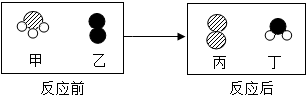
(1)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如图.该反应的前后总共有3种原子.该反应是(填“是”或“不是”)置换反应.反应前后元素的化合价有(填“有”或“无”)变化.在该反应中甲和丁两种分子的个数比为2:3.
(2)胃酸过多须服用抗酸药.如表为两种抗酸药的有效成分及其构成微观粒子:
由于抗酸药有效成分不同,起抗酸作用(即消耗胃液中盐酸)的粒子也有差异.
①Mg(OH)2起抗酸作用的粒子是OH-(填粒子符号,下同);
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑
则铝碳酸镁起抗酸作用的两种粒子是OH-、CO32-.
 化学是在原子、分子、离子水平上研究物质及其变化的科学.
化学是在原子、分子、离子水平上研究物质及其变化的科学.(1)一定条件下,甲和乙反应生成丙和丁(四种物质均由分子构成),反应前后微观示意图如图.该反应的前后总共有3种原子.该反应是(填“是”或“不是”)置换反应.反应前后元素的化合价有(填“有”或“无”)变化.在该反应中甲和丁两种分子的个数比为2:3.
(2)胃酸过多须服用抗酸药.如表为两种抗酸药的有效成分及其构成微观粒子:
| 抗胃酸药 | 复方氢氧化镁片剂 | 铝碳酸镁片 |
| 有效成分 | Mg(OH)2 | AlMg(OH)3CO3 |
| 构成微粒 | Mg2+、OH- | Al3+、Mg2+、OH-、CO32- |
①Mg(OH)2起抗酸作用的粒子是OH-(填粒子符号,下同);
②铝碳酸镁与盐酸的反应为:AlMg(OH)3CO3+5HCl═MgCl2+AlCl3+4H2O+CO2↑
则铝碳酸镁起抗酸作用的两种粒子是OH-、CO32-.
6.2016年3月22日是第二十四届“世界水日”,我国纪念“世界水日”的宣传主题为“落实五大发展理念,推进最严格水资源管理”.下列有关水的说法正确的是( )
| A. | 水可用于灭火 | |
| B. | 淡水资源是取之不尽、用之不竭的 | |
| C. | 可用紫色石蕊试液区分硬水和软水 | |
| D. | 海洋有自净能力,所以不存在海水污染问题 |
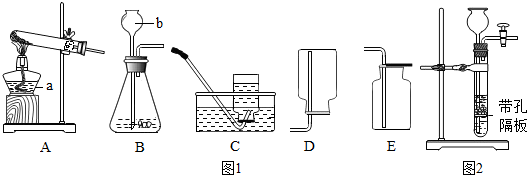
7.下列实验基本操作及仪器装置正确的是( )
| A. |  量筒读数 | B. |  滴加试液 | C. | 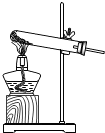 制备氧气 | D. |  过滤操作 |