题目内容
9.随着世界经济的快速增长,对能源的需求也越来越大,核能作为清洁的能源,对于缓解能源紧张局面,减轻环境污染具有积极作用.已知某种核原料的原子核含有1个质子,2个中子,那么( )| A. | 由该原子核形成的单质的相对质量为6 | |
| B. | 该元素是金属元素 | |
| C. | 该原子核外有3个电子 | |
| D. | 该原子核带2个单位的正电荷 |
分析 由题意“已知某种核原料的原子核中含有1个质子和2个中子”,结合“相对原子质量≈质子数+中子数(近似整数值)”和“核内质子数=核外电子数=核电荷数”,根据质子数决定元素种类,推断其原子种类.
解答 解:已知某种核原料的原子核中含有1个质子和2个中子.
A、根据质子数为1,可知该原子是一种氢原子,相对原子质量≈质子数+中子数=1+2=3,因此由该原子核形成的单质的相对质量为6,说法正确;
B、根据质子数为1,可知该元素为氢元素,为非金属元素,说法错误;
C、根据核内质子数=核外电子数可知,该原子核外有1个电子,说法错误;
D、根据原子中质子数等于核外电子数,故原子核外带1个单位的负电荷,说法错误.
故选A.
点评 了解原子的定义和构成:原子由原子核和核外电子构成,其中原子核由质子和中子构成的;掌握元素的概念:具有相同核电荷数(核内质子数)的一类原子的总称.

练习册系列答案
相关题目
1. 元素周期表是学习化学的重要工具,如图是元素周期表中的一格,从该图中,我们获得的相关信息中,错误的是( )
元素周期表是学习化学的重要工具,如图是元素周期表中的一格,从该图中,我们获得的相关信息中,错误的是( )
 元素周期表是学习化学的重要工具,如图是元素周期表中的一格,从该图中,我们获得的相关信息中,错误的是( )
元素周期表是学习化学的重要工具,如图是元素周期表中的一格,从该图中,我们获得的相关信息中,错误的是( )| A. | 该元素的名称是钠 | B. | 该元素的离子Na+结构示意图为 | ||
| C. | 该元素的原子序数为11 | D. | 该元素属于金属元素 |

 日前,世界环保联盟建议全面禁止用氯气对饮用水消毒,推广使用安全、高效杀菌消毒剂ClO2.①ClO2是一种黄绿色、有刺激性气味的气体,②冷却至11.0℃以下时变成红色液体,③易溶于水,④见光易分解,⑤易与碱反应,⑥杀菌、漂白能力均优于氯气.
日前,世界环保联盟建议全面禁止用氯气对饮用水消毒,推广使用安全、高效杀菌消毒剂ClO2.①ClO2是一种黄绿色、有刺激性气味的气体,②冷却至11.0℃以下时变成红色液体,③易溶于水,④见光易分解,⑤易与碱反应,⑥杀菌、漂白能力均优于氯气.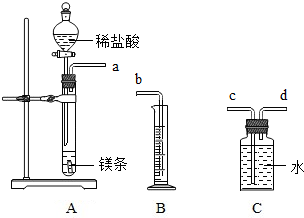 请利用如图给定的仪器组装成一套测定镁的相对原子质量的实验装置(每种仪器只允许使用一次),用排水法测量化学反应产生氢气的体积,根据化学方程式计算出镁的相对原子质量,回答问题:
请利用如图给定的仪器组装成一套测定镁的相对原子质量的实验装置(每种仪器只允许使用一次),用排水法测量化学反应产生氢气的体积,根据化学方程式计算出镁的相对原子质量,回答问题:

