题目内容
1.某纯碱样品中含有少量氯化钠,现欲测定其中碳酸钠的质量分数,进行如下实验:【实验原理】
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑ 通过实验测定反应产生的二氧化碳的质量,即可求得原样品中碳酸钠的质量,进而求得碳酸钠在样品中的质量分数.
【实验步骤】
①按如图所示连接装置(除B、C外)并加入所需药品.
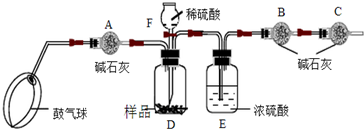
②称量并记录B的质量(m1) (称量时注 意封闭B的两端.)
③挤压鼓气球,持续约1分钟.
④连接上B、C.
⑤打开分液漏斗F的活塞,将稀硫酸快速加入D中后,关闭活塞.
⑥挤压鼓气球,持续约1分钟.
⑦称量并记录B的质量(m2).(称量时注意封闭B的两端及E右端的出口.)
⑧计算.
(1)已知碱石灰的主要成分是氧化钙和氢氧化钠,则干燥管A的作用是除去鼓入空气中的二氧化碳,干燥管C的作用是防止空气中的二氧化碳和水进入B中影响实验结果,E装置的作用是防止D中的水蒸气进入B中.步骤③中鼓气的目的是用除去二氧化碳的空气赶走体系中的二氧化碳;步骤⑥中鼓气的目的是用除去二氧化碳的空气将反应产生的二氧化碳 全部赶入B中;本实验能否同时省略③、⑥两个步骤?不能,原因是①空气中含少量二氧化碳、②反应后装置中残留二氧化碳均会造成结论偏差.
(2)若所取样品的质量为5g,为确保实验顺利进行,分液漏斗F中至少要盛放10%的稀硫酸(密度为1.07g/mL)43.0mL,若m1为51.20 g,m2为53.18g,样品中碳酸钠的质量分数为95.4%.
分析 要测定碳酸钠的含量,可以通过与酸反应生成的二氧化碳的质量进行求算,而要测定二氧化碳的质量,需排除空气中二氧化碳和水蒸气对生成的二氧化碳的质量的影响,除去二氧化碳使用的是氢氧化钠溶液,除去水使用的是浓硫酸.
解答 解:(1)干燥管A可以吸收鼓气球中鼓入的空气中的二氧化碳,避免对干燥管B的质量增加造成干扰;干燥管Ⅱ在干燥管I之后,能阻止空气中的二氧化碳和水进入干燥管,E中盛有的是浓硫酸,具有吸水性,能将水分吸除,排除水分对生成二氧化碳质量的影响;步骤③中鼓气的目的是用除去二氧化碳的空气赶走体系中的二氧化碳,步骤⑥鼓入空气是利用压力差使产生的二氧化碳全部被排出,要测定二氧化碳的质量,需排除空气中二氧化碳对生成的二氧化碳的质量的影响;本实验不能同时省略③、⑥两个步骤,否则会给实验带来误差.
(2)当5克样品全部为碳酸钠时,耗硫酸最多,设所需硫酸的质量为x
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
106 98
5 x
$\frac{106}{5}=\frac{98}{x}$
x=4.6(g)
故至少要盛放10%的稀硫酸(密度为1.07g/mL)的体积为:V=$\frac{\frac{4.6g}{10%}}{1.07}$≈43.0(ml)
根据所测数据,生成二氧化碳的质量为(m2-m1)=1.98g,设碳酸钠的质量为x,则有
Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
106 44
X 1.98g
$\frac{106}{x}=\frac{44}{1.98g}$
x=4.77(g)
所以纯碱样品纯度为:$\frac{4.77g}{5g}$×100%=95.4%
故答案为:
(1)除去鼓入空气中的二氧化碳;防止空气中的二氧化碳和水进入B中影响实验结果;防止D中的水蒸气进入B中;用除去二氧化碳的空气赶走体系中的二氧化碳;用除去二氧化碳的空气将反应产生的二氧化碳 全部赶入B中;不能;①空气中含少量二氧化碳、②反应后装置中残留二氧化碳均会造成结论偏差.
(2)43.0;95.4%.
点评 本题考查了碳酸钠含量的测定,完成此题,可以依据生成的二氧化碳的质量进行求算,进行实验时,要保证生成的二氧化碳的质量准确.

 阅读快车系列答案
阅读快车系列答案| A. | 水壶底部的水垢,可以用NaOH溶液浸泡除去 | |
| B. | 汽车修理工用汽油洗去手上的油污,是乳化作用的 结果 | |
| C. | 增大空气与水的接触面积,不能增大氧气的溶解度 | |
| D. | 析出晶体后的溶液不一定是饱和溶液 |
| A. | 氧化剂 | B. | 催化剂 | C. | 还原剂 | D. | 反应物 |
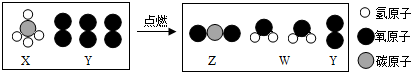
| A. | X是有机物,Z、W是无机物 | |
| B. | 生成物都是氧化物 | |
| C. | 该反应的化学方程式CH4+O2$\frac{\underline{\;点燃\;}}{\;}$CO2+H2O | |
| D. | 点燃X前,要先检验其纯度,以防止爆炸 |
| A. | 尽量使用节能技术和节能用具 | B. | 尽量使用公共交通工具或步行 | ||
| C. | 尽量使用一次性餐筷和塑料餐具 | D. | 广泛使用太阳能和风能等清洁能源 |
| A. | 在化学变化中,分子可以分原子不可再分 | |
| B. | 分子大、原子小 | |
| C. | 分子间有间隔,原子间没有间隔 | |
| D. | 分子在不停地运动,原子不运动 |
查得资料:该牙膏摩擦剂主要由碳酸钙、氢氧化铝组成;其他成分遇到盐酸时无气体生成.
方案设计:小组的两位同学提出了各自的设计方案
甲同学:利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.
乙同学:也利用图示装置进行实验,充分反应后,测定C装置中反应前后的质量差,得出二氧化碳质量,以确定碳酸钙的质量分数.
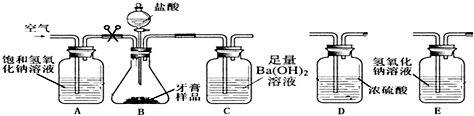
小组同学认为甲同学装置还需要进一步完善,在C装置后他们又增加了一个装置,你认为他们增加的装置是E(选填D或E),其目的是防止空气中的二氧化碳进入C装置影响实验测定.同时小组同学经过讨论后认为乙同学的设计存在明显的缺陷,你认为此缺陷是挥发的氯化氢气体等也进入了C装置.
实验步骤:(1)检查装置气密性(2)打开止水夹,缓缓通入一段时间空气(3)关闭止水夹,打开分液漏斗活塞(4)再次打开止水夹,缓缓通入一段时间空气(5)过滤出沉淀,进行适当的处理后称量其质量.实验过程中,C装置应该在实验步骤2后(填序号)与B装置连接,否则实验结果偏大 (填偏大、偏小或无影响).
进行实验:同学们分四组准确称取四份样品,每份均为16.00g,按照实验步骤分别进行实验,得到了如下的实验数据:
| 组别 | 第一组 | 第二组 | 第三组 | 第四组 |
| 沉淀质量(g) | 7.86 | 7.88 | 7.90 | 9.86 |
A.实验结束后通入空气速度太快,装置中的二氧化碳没有完全吸收
B.沉淀过滤后没有洗涤
C.沉淀没有干燥直接称量
D.称量沉淀质量时,砝码与药品位置放反了
(2)根据另外三组同学的BaCO3平均质量,计算出了收集到的二氧化碳质量为1.76g.
(3)计算该样品中碳酸钙的质量分数?(写出计算过程)
实验反思:实验后,有同学提出用氢氧化钙溶液替代氢氧化钡溶液可以直接得到碳酸钙沉淀,称量其质量后即可算出质量分数.大家讨论后认为用氢氧化钡溶液比氢氧化钙更好,请说出他们的理由氢氧化钡的溶解性大于氢氧化钙,更容易完全吸收二氧化碳(答出一点即可).