题目内容
下列是初中化学常见的四个实验,回答下列问题: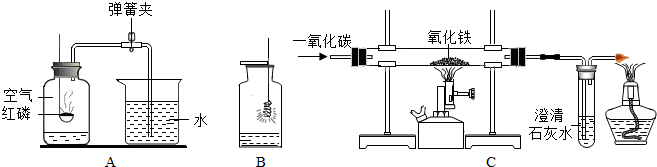
(1)A中可燃物应取过量的原因是 ;实验中导致实验结果偏小的原因是 (只写一个).
(2)B实验中集气瓶内预先装少量水的目的是 .
(3)C实验中红棕色粉末变 ,该处所发生反应的化学方程式: .C中酒精灯的作用是 .

(1)A中可燃物应取过量的原因是
(2)B实验中集气瓶内预先装少量水的目的是
(3)C实验中红棕色粉末变
考点:空气组成的测定,氧气的化学性质,一氧化碳还原氧化铁,书写化学方程式、文字表达式、电离方程式
专题:实验性简答题
分析:(1)从测定空气中氧气含量的实验原理去分析解答;
(2)从铁丝在氧气中燃烧的实验,由于铁丝燃烧时会产生大量的热,产生的高温溶化物,如果落到集气瓶的底部,会使集气瓶底部因局部温度过高而炸裂去分析解答;
(3)从一氧化碳和红棕色氧化铁在高温下生成铁(纯铁是银白色的,此时产生的还原铁粉是黑色的)和二氧化碳,如何防止CO污染空气去分析解答.
(2)从铁丝在氧气中燃烧的实验,由于铁丝燃烧时会产生大量的热,产生的高温溶化物,如果落到集气瓶的底部,会使集气瓶底部因局部温度过高而炸裂去分析解答;
(3)从一氧化碳和红棕色氧化铁在高温下生成铁(纯铁是银白色的,此时产生的还原铁粉是黑色的)和二氧化碳,如何防止CO污染空气去分析解答.
解答:解:(1)图A是测定空气中氧气含量的实验.实验原理:利用红磷燃烧消耗空气中的氧气,使左边集气瓶内气体体积变小,压强变小,从而在外部大气压的作用下使烧杯内的水进入集气瓶,通过测量进入集气瓶中水的量来确定空气中氧气的体积分数.①实验过程中要加入过量的红磷,如果所用红磷的量不足,使瓶内空气中的氧气没有完全被消耗,会使所测得的氧气的体积分数偏小;②如果装置漏气,会使外界的空气进入集气瓶,导致进入集气瓶内的水的体积变小,导致实验偏小;故答案为:将集气瓶中的氧气全部消耗掉 装置漏气;
(2)图B是铁丝在氧气中燃烧的实验,由于铁丝燃烧时会产生大量的热,产生高温溶化物,如果落到集气瓶的底部,会使集气瓶底部因局部温度过高而炸裂;故答案为:防止铁丝燃烧后的熔化物溅落炸裂集气瓶底部;
(3)图C是一氧化碳还原氧化铁的实验.一氧化碳和红棕色氧化铁在高温下生成铁(纯铁是银白色的,此时产生的还原铁粉是黑色的)和二氧化碳;其化学方程式为:Fe2O3+3CO
2Fe+3CO2;由于CO是空气污染物之一,为防止实验过程中没有反应的CO跑到外界污染空气,要把尾气进行处理,处理的方法是把尾气点燃转化成为二氧化碳;故答案为:黑; Fe2O3+3CO
2Fe+3CO2 防止CO污染空气.
(2)图B是铁丝在氧气中燃烧的实验,由于铁丝燃烧时会产生大量的热,产生高温溶化物,如果落到集气瓶的底部,会使集气瓶底部因局部温度过高而炸裂;故答案为:防止铁丝燃烧后的熔化物溅落炸裂集气瓶底部;
(3)图C是一氧化碳还原氧化铁的实验.一氧化碳和红棕色氧化铁在高温下生成铁(纯铁是银白色的,此时产生的还原铁粉是黑色的)和二氧化碳;其化学方程式为:Fe2O3+3CO
| ||
| ||
点评:纯铁是银白色的,但一氧化碳还原氧镄铁产生的还原铁粉是黑色的.

练习册系列答案
相关题目
如表是元素周期表的一部分,则下列回答正确的是( )
| 11 Na 钠 | 12 Mg 镁 | 13 Al 铝 | 14 Si 硅 | 15 P 磷 | 16 S 硫 | 17 Cl 氯 | 18 Ar 氩 |
| A、12号元素的离子符号是Mg+2 |
B、氯原子的核外电子排布是 ,则氯原子容易得一个电子达到稳定结构 ,则氯原子容易得一个电子达到稳定结构 |
| C、表中左边是非金属元素、右边是金属元素 |
| D、硫元素的相对原子质量为16 |
逻辑推理是化学学习中常用的思维方法.下列推理正确的是( )
| A、中和反应生成盐和水,则生成盐和水的反应一定是中和反应 |
| B、盐是由金属离子和酸根离子组成的,NH4NO3中没有金属离子,不属于盐 |
| C、化合物是由不同种元素组成的纯净物.所以由不同种元素组成的纯净物一定是化合物 |
| D、活泼金属能与稀硫酸反应放出气体,则能与稀硫酸反应放出气体的物质一定是活泼金属 |
下列关于溶液的说法正确的是( )
| A、溶液一定是均一、稳定、澄清、无色的 |
| B、饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液 |
| C、同种溶质的饱和溶液,一定比它的不饱和溶液溶质质量分数大 |
| D、不饱和溶液转化为饱和溶液,溶质质量分数不一定变 |
下列厨房中的物质(或其主要成分)由离子构成的是( )
| A、食盐 | B、蔗糖 | C、植物油 | D、白酒 |