题目内容
实验小组研究盐酸、氢氧化钠、氢氧化钙三种物质的化学性质,做了如图所示的实验.请你利用图中所给药品和他们一起进行研究.
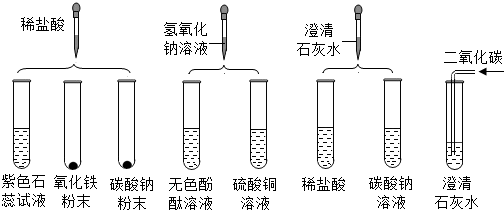
(1)实验后某试管中为黄色溶液,该试管中发生反应的化学方程式为 .
(2)实验后某试管中为红色溶液,向其中加入足量的 ,溶液变为无色.由此推断,该试管中最初盛有的物质是 .
(3)实验后某试管底部有蓝色絮状沉淀,继续向其中加入足量的 ,振荡后沉淀消失.
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加稀盐酸,开始时无明显现象,一段时间后有气泡出现.由此推断,该试管中最初发生反应的化学方程为 .
(5)实验后某试管中只得到无色溶液,向其中加入足量的碳酸钠溶液,只产生气泡.那么该试管中最初发生反应的化学方程为 .
(6)实验结束时,他们将实验废液倒入同一废液缸中,观察后,他们猜想最终的废液可能呈酸性.为了验证猜想,利用上述实验中未涉及到的酸的化学性质,另选药品进行实验:取少量废液样品于试管中,向其中加入一定量的 ,观察现象,证明最终的废液呈酸性.实验后为了避免废液造成不良后果,他们对废液进行了恰当处理.

(1)实验后某试管中为黄色溶液,该试管中发生反应的化学方程式为
(2)实验后某试管中为红色溶液,向其中加入足量的
(3)实验后某试管底部有蓝色絮状沉淀,继续向其中加入足量的
(4)实验后某试管的底部有白色固体,过滤后向滤液中滴加稀盐酸,开始时无明显现象,一段时间后有气泡出现.由此推断,该试管中最初发生反应的化学方程为
(5)实验后某试管中只得到无色溶液,向其中加入足量的碳酸钠溶液,只产生气泡.那么该试管中最初发生反应的化学方程为
(6)实验结束时,他们将实验废液倒入同一废液缸中,观察后,他们猜想最终的废液可能呈酸性.为了验证猜想,利用上述实验中未涉及到的酸的化学性质,另选药品进行实验:取少量废液样品于试管中,向其中加入一定量的
考点:探究酸碱的主要性质,酸的化学性质,碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)根据氧化铁和稀盐酸反应生成氯化铁和水,氯化铁溶于水呈黄色分析;
(2)根据碱能使酚酞变色、碱和稀盐酸反应生成盐和水、盐和酸都不能使酚酞变色分析;
(3)根据氢氧化钠与硫酸铜反应生成蓝色沉淀,加盐酸蓝色沉淀溶解分析;
(4)根据氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠分析;
(5)根据碳酸钠和稀盐酸反应生成气体分析;
(6)根据活泼金属能与酸反应生成气体分析.
(2)根据碱能使酚酞变色、碱和稀盐酸反应生成盐和水、盐和酸都不能使酚酞变色分析;
(3)根据氢氧化钠与硫酸铜反应生成蓝色沉淀,加盐酸蓝色沉淀溶解分析;
(4)根据氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠分析;
(5)根据碳酸钠和稀盐酸反应生成气体分析;
(6)根据活泼金属能与酸反应生成气体分析.
解答:解:解:氧化铁和稀盐酸反应生成氯化铁和水,氯化铁溶于水呈黄色,故化学方程式为:Fe2O3+6HCl=2FeCl3+3H2O;
(2)氢氧化钙能使酚酞变红色,稀盐酸和氢氧化钙反应生成氯化钙、水和二氧化碳,稀盐酸有可能过量但氯化钙和稀盐酸都不能使酚酞变色;
(3)氢氧化钠与硫酸铜反应生成蓝色沉淀,加盐酸蓝色沉淀溶解;
(4)氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(5)碳酸钠和稀盐酸反应生成气体二氧化碳,故化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(6)活泼金属能与酸反应生成气体,故取少量废液样品于试管中,向其中加入一定量的铁粉,若产生气泡,则证明溶液呈酸性.
故答案为:(1)Fe2O3+6HCl=2FeCl3+3H2O;
(2)稀盐酸;无色酚酞溶液;
(3)稀盐酸;
(4)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(5)Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(6)铁粉
(2)氢氧化钙能使酚酞变红色,稀盐酸和氢氧化钙反应生成氯化钙、水和二氧化碳,稀盐酸有可能过量但氯化钙和稀盐酸都不能使酚酞变色;
(3)氢氧化钠与硫酸铜反应生成蓝色沉淀,加盐酸蓝色沉淀溶解;
(4)氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,故化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(5)碳酸钠和稀盐酸反应生成气体二氧化碳,故化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(6)活泼金属能与酸反应生成气体,故取少量废液样品于试管中,向其中加入一定量的铁粉,若产生气泡,则证明溶液呈酸性.
故答案为:(1)Fe2O3+6HCl=2FeCl3+3H2O;
(2)稀盐酸;无色酚酞溶液;
(3)稀盐酸;
(4)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(5)Na2CO3+2HCl=2NaCl+H2O+CO2↑;
(6)铁粉
点评:本题综合考查了酸碱的化学性质的探究,全面综合的考查,角度新颖,解答时抓住酸碱的化学性质不难解答.

练习册系列答案
相关题目
生活中处处充满化学,下列生活中的化学知识叙述不正确的是( )
| A、建筑工地上盛有石灰水的池中常会看到一层白膜,该白膜是氢氧化钙 |
| B、在厨房中可以用品尝的方法鉴别食盐与味精 |
| C、用食醋进行熏蒸可以消毒杀菌 |
| D、医疗上可用一定质量分数的葡萄糖溶液给病人输液以补充能量 |
 化学和生产、生活紧密相关.请你用所学知识回答下列问题.
化学和生产、生活紧密相关.请你用所学知识回答下列问题.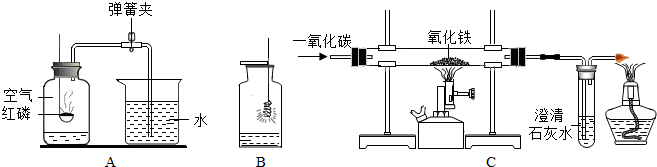

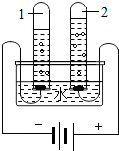 3月22日是“世界水日”,水与人类的生活和生产密切相关.
3月22日是“世界水日”,水与人类的生活和生产密切相关.