题目内容
20.碳和金属形成的化合物叫碳化物.某碳化物MC2中碳元素含量为37.5%,已知C的相对原子质量为12,则金属M的相对原子质量为40.分析 根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答.
解答 解:某碳化物MC2中碳元素含量为37.5%,已知C的相对原子质量为12,则该碳化物的相对分子质量为12×2÷37.5%=64.
金属M的相对原子质量为64-12×2=40.
故答案为:40.
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 口算题天天练系列答案
口算题天天练系列答案
相关题目
8.下列仪器中能直接加热的玻璃仪器是( )
| A. | 试管 | B. | 燃烧匙 | C. | 蒸发皿 | D. | 烧杯 |
15.下列依据实验目的所设计的实验操作中,正确的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 检验NaOH中是否含有Na2CO3 | 滴加少量稀盐酸 |
| B | 鉴别NaOH和Ca(OH)2溶液 | 加Na2CO3溶液 |
| C | 清洗铁制品表面的铁锈 | 用水洗涤 |
| D | 除去CO2中的CO | 通入足量的澄清石灰水中 |
| A. | A | B. | B | C. | C | D. | D |
5.下列做法存在安全隐患的是( )
| A. | 炒菜时油锅着火,立刻盖上锅盖 | |
| B. | 维修沼气池前,先做灯火实验 | |
| C. | 室内发生火灾,应打开所有门窗通风 | |
| D. | 发现液化气泄漏,关闭阀门并开窗通风 |
9.下列叙述正确的是( )
| A. | 氧化反应都发光、放热 | |
| B. | 氦气用于填充食品包装袋中,延长保质期 | |
| C. | 鱼能在水中生存,是由于氧气易溶于水 | |
| D. | 按体积分数计算,呼出气体中氮气最高 |
10.测大理石纯度,取400克稀盐酸等分为4等份
M=6.6克,哪几次大理石过量第四次,大理石纯度50%,稀盐酸纯度11.6%,完成.
| 第一份 | 第二份 | 第三份 | 第四份 |
| 大理石 10克 | 20克 | 30克 | 40克 |
| CO2 2.2克 | 4.4克 | M | 7克 |
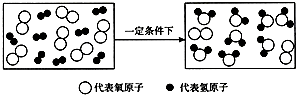 如图是某化学变化的微观示意图.
如图是某化学变化的微观示意图.