题目内容
4.下列各组物质间能发生化学反应的是( )| A. | 银和稀盐酸 | B. | 铁和硫酸锌溶液 | ||
| C. | 硝酸钾溶液和食盐水 | D. | 硫酸和氯化钡溶液 |
分析 利用金属活动性顺序以及复分解反应的发生条件解决此题,能否反应要熟悉金属活动性顺序以及意义、生成物中是否有水沉淀或气体,还要对反应特别是盐与盐、盐与碱的反应中反应物均可溶作出判断.
解答 解:A、银在氢的后面,不能与盐酸反应,错误;
B、铁在锌的后面,不能与硫酸锌反应,错误;
C、硝酸钾和食盐交换成分没有沉淀、气体和水生成,不能发生反应,错误;
D、硫酸和氯化钡交换成分能生成硫酸钡沉淀,能发生反应,正确;
故选D.
点评 此题是对化学反应进行的判断题,解题的关键是抓住金属活动性顺序的意义以及复分解反应的发生条件进行判断分析即可.

练习册系列答案
相关题目
6.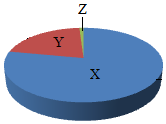 图为空气成分示意图(按体积分数计算),其中“X”代表的是( )
图为空气成分示意图(按体积分数计算),其中“X”代表的是( )
 图为空气成分示意图(按体积分数计算),其中“X”代表的是( )
图为空气成分示意图(按体积分数计算),其中“X”代表的是( )| A. | 氮气 | B. | 氧气 | C. | 二氧化碳 | D. | 稀有气体 |
13.大自然中学锦绣同学向2g碳酸钠、氢氧化钠、氧化钙的混合物中加入100g水,混合后恰好完全反应后过滤,将滤液蒸干,滤液减少的质量为99.82g,则锦绣同学所取混合物中碳酸钠和氢氧化钠的质量比为( )
| A. | 53:40 | B. | 53:19 | C. | 53:80 | D. | 53:28 |
16.用饱和食盐水和碳酸氢铵反应可以获得碳酸氢钠:NH4HCO3+NaCl═NaHCO3↓+NH4Cl(20℃时,NH4HCO3溶解度为21g,NaCl溶解度为36g,NaHCO3溶解度为9.6g).下列关于该反应的叙述正确的是( )
| A. | NaHCO3是碱 | |
| B. | 该反应中四种物质都是盐 | |
| C. | 该反应不符合复分解反应发生的条件 | |
| D. | 析出晶体后剩余溶液中的溶质只有NH4Cl一种 |
13.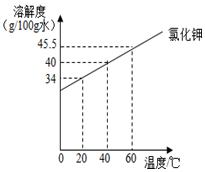 根据下表实验,回答相关问题
根据下表实验,回答相关问题
①实验步骤Ⅱ中加入Xg氯化钾,X=9g.
②实验步骤Ⅲ中所得溶液是饱和(填“饱和”或“不饱和”)溶液.
③冷却至20℃,烧杯中的现象是有固体析出.
④有五瓶氯化钾溶液,与上述实验步骤Ⅰ-Ⅴ形成的溶液溶质质量分数分别相等,现各取10g于5个小烧杯中,分别滴入足量的等质量等浓度的硝酸银溶液,其中有3个小烧杯中产生的沉淀质量相等.
 根据下表实验,回答相关问题
根据下表实验,回答相关问题| 实验步骤 | 实验操作 | 实验现象 |
| Ⅰ | 在盛有100g水的烧杯中,加入25g氯化钾,搅拌,恢复到20℃. | 全部溶解 |
| Ⅱ | 再加Xg氯化钾,搅拌,恢复到20℃,恰好饱和. | 全部溶解 |
| Ⅲ | 再加6g氯化钾,搅拌,恢复到20℃ | 固体不溶 |
| Ⅳ | 加热 | 全部溶解 |
| Ⅴ | 冷却至20℃ | 有固体析出 |
②实验步骤Ⅲ中所得溶液是饱和(填“饱和”或“不饱和”)溶液.
③冷却至20℃,烧杯中的现象是有固体析出.
④有五瓶氯化钾溶液,与上述实验步骤Ⅰ-Ⅴ形成的溶液溶质质量分数分别相等,现各取10g于5个小烧杯中,分别滴入足量的等质量等浓度的硝酸银溶液,其中有3个小烧杯中产生的沉淀质量相等.

 如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“-”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同,D是一种红色粉末,F是相对分子质量最小的氧化物.请回答下列问题.
如图所示A~G是初中化学中常见的物质(反应条件和部分产物已省略,“-”表示相互能反应,“→”表示转化关系),其中A是人体胃液中含有的酸,B与C的组成元素相同,D是一种红色粉末,F是相对分子质量最小的氧化物.请回答下列问题.