题目内容
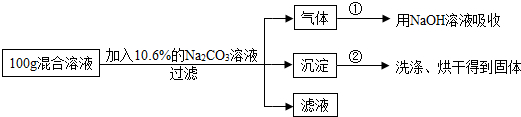
20.某纯碱样品中混有少量的氯化钠,为了测定样品的纯度,小明做了如下实验:准确称取样品12.0g,并将100g稀盐酸分四次加入,每次加入情况如表,请回答下列问题:| 实验次数 | 一 | 二 | 三 | 四 |
| 所加盐酸的量/g | 25 | 25 | 26 | 25 |
| 产生气体的质量/g | 1.32 | m | 1.32 | 0 |
(2)纯碱样品中的Na2CO3的质量分数是多少?
(3)当纯碱与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数为多少?(精确到0.01%)
分析 (1)由图可知,每加入15g盐酸生成1.32g二氧化碳,第四次加入盐酸仍有气体生成,说明第三次中的盐酸全部反应,生成1.32g气体,则m的值为1.32;
(2)第四次加入的盐酸有剩余,则12g样品完全反应生成二氧化碳的量为:1.32g+1.32g+1.32g+0.44g=4.4g;根据化学方程式和二氧化碳的质量即可求出碳酸钠的质量,进而求其质量分数.
解答 解:(1)由图可知,每加入25g盐酸生成1.32g二氧化碳,第四次加入盐酸仍有气体生成,说明第三次中的盐酸全部反应,生成1.32g二氧化碳气体,则m的值为1.32;
故答案为:1.32;
(2)第四次加入的盐酸有剩余,则12g样品完全反应生成二氧化碳的量为:1.32g+1.32g+1.32g=3.96g;
设纯碱样品中的Na2CO3的质量为x,恰好完全反应时,生成氯化钠的质量为y;
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 117 44
x y 3.96g
$\frac{106}{x}=\frac{117}{y}=\frac{44}{3.96g}$
x=9.54g
y=10.53g
纯碱样品中的Na2CO3的质量分数是:$\frac{9.54g}{12g}×100%$=79.5%
答:纯碱样品中的Na2CO3的质量分数是79.5%.
(3)当纯碱与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数为:$\frac{10.53g}{12g+75g-3.96g}$×100%=12.68%;
答:所得溶液中溶质的质量分数为12.68%.
点评 会正确分析图表所给信息是正确解决本题的关键.

练习册系列答案
相关题目
10.除去下列物质中的杂质,所选用的试剂和操作方法都正确的是( )
| 选项 | 物质 | 杂质(少量) | 试剂及操作方法 |
| A | 稀盐酸 | 稀硫酸 | 加入过量的氯化钡溶液,过滤 |
| B | 氧化钙 | 石灰石 | 高温 |
| C | 氯化钠 | 泥沙 | 加入足量的水溶解、蒸发、结晶 |
| D | 氨气 | 水蒸气 | 通过足量的氢氧化钠固体干燥剂 |
| A. | A | B. | B | C. | C | D. | D |
8.改变20℃时硝酸钾饱和溶液的质量分数,可行的方法是( )
| A. | 恒温蒸发少量溶剂 | B. | 加入硝酸钾固体 | ||
| C. | 降低温度到10℃ | D. | 升高温度到30℃ |
15.下列实验能达到目的是( )
| A. | 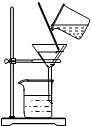 分离溶液中NaCl和CaCl2两种溶质 | B. | 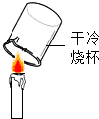 检验蜡烛中是否含有氢元素 | ||
| C. | 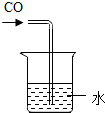 用水吸收CO | D. | 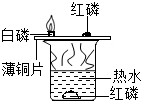 探究燃烧的条件 |
12.下列实验方案设计正确的是( )
| 选项 | 实验目的 | 方案 |
| A | 检验氧气是否收集满 | 将带火星的木条伸入集气瓶内 |
| B | 除去甲烷中混有的一氧化碳 | 点燃 |
| C | 鉴别稀盐酸和NaCl溶液 | 分别滴加酚酞试液 |
| D | 除去木炭粉中混有的少量氧化铜 | 加入适量稀硫酸,充分反应后,过滤,洗涤,干燥 |
| A. | A | B. | B | C. | C | D. | D |
16.能用作是复合肥的是( )
| A. | NaCl | B. | KNO3 | C. | Ca 3(PO4)2 | D. | NH4Cl |