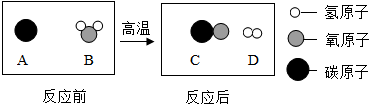
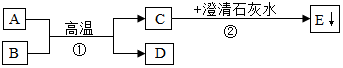
题目内容
15.下列实验能达到目的是( )| A. | 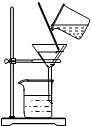 分离溶液中NaCl和CaCl2两种溶质 | B. | 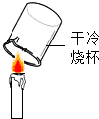 检验蜡烛中是否含有氢元素 | ||
| C. | 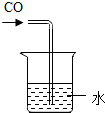 用水吸收CO | D. | 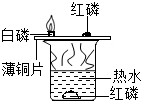 探究燃烧的条件 |
分析 A、根据氯化钠和氯化钙都溶于水分析;
B、根据现象结合元素种类不变分析;
C、根据CO不溶于水的物理性质分析即可;
D、运用了对比的实验方法,得出可燃物燃烧的条件.
解答 解:A、氯化钠和氯化钙都溶于水,因此不能采用过滤法分离,故错误;
B、干冷的烧杯内壁有水珠产生,说明蜡烛中含有氢元素,故正确;
C、CO不溶于水,所以不能用水吸收,故错误;
D、热水中的红磷和薄铜片上的红磷都不能燃烧,不能得出燃烧需要氧气的条件,故错误;
故选项为:B.
点评 本题是有关实验方案的设计和评价的考查,要求学生熟悉所实验的内容及原理,能够考查同学们进行分析问题、解决问题的能力.

练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
6.2015年3月5日备受社会关注的“PM2.5”一词出现在政府工作报告中,治理大气的环境问题成为我国政府工作的重点之一,下列做法不利于保护大气环境的是( )
| A. | 春节假日,多燃放染化及爆竹 | B. | 上学上班,多乘坐公交车出行 | ||
| C. | 春耕播种,适量施肥肥沃土壤 | D. | 万物复苏,多植树造林护大气 |
20.某纯碱样品中混有少量的氯化钠,为了测定样品的纯度,小明做了如下实验:准确称取样品12.0g,并将100g稀盐酸分四次加入,每次加入情况如表,请回答下列问题:
(1)m的值是1.32;
(2)纯碱样品中的Na2CO3的质量分数是多少?
(3)当纯碱与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数为多少?(精确到0.01%)
| 实验次数 | 一 | 二 | 三 | 四 |
| 所加盐酸的量/g | 25 | 25 | 26 | 25 |
| 产生气体的质量/g | 1.32 | m | 1.32 | 0 |
(2)纯碱样品中的Na2CO3的质量分数是多少?
(3)当纯碱与稀盐酸恰好完全反应时,所得溶液中溶质的质量分数为多少?(精确到0.01%)
7.下列关于水的说法正确的是( )
| A. | 水由氢分子和一个氧原子构成 | B. | 活性炭可将自来水转化为纯水 | ||
| C. | 水受热蒸发,水分子体积增大 | D. | 电解水可证明水由氢、氧元素组成 |
11.下列实验现象描述错误的是( )
| A. | 红磷在氧气中燃烧,产生大量的白雾 | |
| B. | 硫在氧气中燃烧发出明亮的蓝紫色火焰 | |
| C. | 铁在氧气中剧烈燃烧,火星四射,生成黑色固体 | |
| D. | 铝丝浸入硫酸铜溶液中,表面有红色物质析出 |
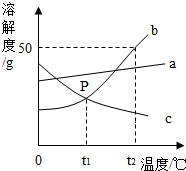 根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据如图中a、b、c三种物质的溶解度曲线,回答下列问题: A、B、C、D、E分别是稀盐酸、硝酸银溶液、碳酸钠溶液、氢氧化钡溶液、铁粉中的一种物质,相切的两椭圆表示它们之间能发生反应,它们之间的部分反应链接起来可形成美丽的蝴蝶,请回答下列问题:
A、B、C、D、E分别是稀盐酸、硝酸银溶液、碳酸钠溶液、氢氧化钡溶液、铁粉中的一种物质,相切的两椭圆表示它们之间能发生反应,它们之间的部分反应链接起来可形成美丽的蝴蝶,请回答下列问题: