题目内容
12.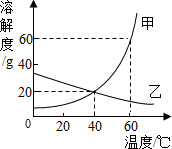 如图是甲、乙两种物质的溶解度曲线,则下列叙述正确的是( )
如图是甲、乙两种物质的溶解度曲线,则下列叙述正确的是( )| A. | 可用100g水配制60℃时溶液质量为180g的甲溶液 | |
| B. | 40℃时,甲、乙两物质溶液的溶质质量分数一定相等 | |
| C. | 升高温度可以将乙的饱和溶液转化为不饱和溶液 | |
| D. | 50℃时,甲物质的溶解度大于乙物质的溶解度 |
分析 A、据该温度下甲的溶解度分析解答;
B、不知溶液中溶质、溶剂的质量,无法判断溶液中溶质的质量分数大小;
C、据乙的溶解度随温度升高而减小分析解答;
D、据溶解度曲线可比较同一温度下不同物质的溶解度大小.
解答 解:A.由图示可知,60℃时甲物质的溶解度是60g,即100g水中最多溶解60g的甲,故用100g水在60℃时最多溶解60g甲物质,所得溶液质量为160g的溶液,不是180g,故错误;
B.40℃时,甲、乙两物质的溶解度相同,故甲、乙饱和溶液的溶质质量分数一定相等,但选项不知溶液是否饱和,则不知溶液中溶质、溶剂的质量,故无法判断溶质的质量分数;错误;
C.由图示可知,乙的溶解度随温度的升高而减小,所以它的饱和溶液降温才能变为不饱和;错误;
D.由图示可知,50℃时,甲物质的溶解度大于乙物质的溶解度;正确;
故选:D.
点评 本题主要考查了对固体溶解度的概念的理解和固体溶解度曲线的意义,以此培养学生的理解能力、培养学生分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.如图所示的实验操作中,正确的是( )
| A. |  细铁丝燃烧 | B. |  稀释浓硫酸 | C. |  倾倒液体 倾倒液体 | D. |  点燃酒精灯 |
20.下表是NaOH和Ca(OH)2的溶解度数据,请回答下列问题.
(1)从表中数据可以获得的信息是氢氧化钠的溶解度随温度升高而增大(写一条).
(2)把80℃时NaOH的饱和溶液降温至20℃,可以看到的现象是有晶体析出,此时溶液的溶质质量分数为47.9%.(保留一位小数)
(3)某兴趣小组对部分变质的氢氧化钠固体进行提纯,设计了如下操作流程:请回答:

(Ⅰ)步骤②中加入过量Ca(OH)2的目的是使Na2CO3充分反应;
涉及反应的化学方程式为_Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(Ⅱ)滤液B中的溶质是Ca(OH)2、NaOH(写化学式);
步骤③所包含的具体操作是加热浓缩、降温、过滤.
(Ⅲ)若实验前称得样品的质量为10g,实验后称得“滤渣A”和“NaOH固体”的质量分别是5g和8.7g,则此样品的纯度为47%.
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度 (g) | NaOH | 31 | 91 | 111 | 129 | 313 | 336 |
| Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 | |
(2)把80℃时NaOH的饱和溶液降温至20℃,可以看到的现象是有晶体析出,此时溶液的溶质质量分数为47.9%.(保留一位小数)
(3)某兴趣小组对部分变质的氢氧化钠固体进行提纯,设计了如下操作流程:请回答:

(Ⅰ)步骤②中加入过量Ca(OH)2的目的是使Na2CO3充分反应;
涉及反应的化学方程式为_Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
(Ⅱ)滤液B中的溶质是Ca(OH)2、NaOH(写化学式);
步骤③所包含的具体操作是加热浓缩、降温、过滤.
(Ⅲ)若实验前称得样品的质量为10g,实验后称得“滤渣A”和“NaOH固体”的质量分别是5g和8.7g,则此样品的纯度为47%.
17.下列关于“水”的变化,属于化学变化的是( )
| A. | 配制食盐水 | B. | 过滤河水 | ||
| C. | 冰融化成雪水 | D. | 雨水在空中形成酸雨 |
4.下列固体放于水后,溶液温度明显升高的是( )
①氢氧化钠 ②氯化钠 ③硝酸铵 ④生石灰.
①氢氧化钠 ②氯化钠 ③硝酸铵 ④生石灰.
| A. | ①④ | B. | ①②③④ | C. | ①② | D. | ①②③ |
1.工业生产的尾气中含有CO、HCl、CO2、粉尘、水蒸气.小刚同学认为这样的尾气需要以下试剂及方法处理:①用浓硫酸洗涤;②用水洗并对液体过滤;③石灰乳吸收.下列对小刚设计方案的讨论意见中正确的是( )
| A. | ①②③是正确的除杂去污的顺序 | |
| B. | 经上述处理后的气体可向空气中排放 | |
| C. | 用烧碱代替石灰乳一定能降低成本 | |
| D. | 经②③①后可回收酸液、燃料再利用 |


