题目内容
1.小明发现家中一枚戒指生满了铜绿,他和同学利用这枚戒指展开了研究性学习.[查阅资料]
(1)真金在空气中不会生锈,生满铜绿的“金戒指”材质为铜锌合金;铜长期露置在潮湿的空气中能生成铜绿,其主要成分是碱式碳酸铜【化学式为Cu2(OH)2CO3】,碱式碳酸铜受热易分解生成CuO、H2O和CO2.据上述资料可推知,碱式碳酸铜由4种元素组成.
(2)Cu2(OH)2CO3+4HCl=2CuCl2+3H2O+CO2↑
[实验探究]将该枚戒指加入过量稀盐酸中,有气泡产生,溶液由无色逐渐变为蓝绿色.
(1)小明认为:气体中除了含有CO2,还可能含有少量H2,实验室常用燃着的木条,点燃的方法检验这种可能含有的气体.
(2)小红认为蓝绿色溶液中的溶质只有氯化锌,小华认为溶液中的溶质除了氯化锌外,还应该含有CuCl2、HCl.他取适量上述蓝绿色溶液,加入光亮的铁片,观察到了现象:①有气泡产生,②有红色物质析出(溶液颜色变浅),证实了自己的观点.
(3)小娟取适量新制的FeCl2溶液,加入锌粒,一段时间后,溶液颜色变浅.结合小华的实验可推知:铁、锌、铜三种金属的活动性由弱到强的顺序是Cu<Fe<Zn.
分析 [查阅资料]根据化学反应前后元素种类不发生改变分析解答;
[实验探究](1)根据戒指的成分可以做出推断;
(2)从戒指的成分和探究过程中加入过量的酸可知,溶液中还含有氯化铜和盐酸,这两种物质都能和锌反应并伴随不同的现象,可以据此解答;
(3)根据锌和氯化亚铁反应生成铁和氯化锌,铁能置换氯化铜中的铜分析解答.
解答 解:[查阅资料]碱式碳酸铜受热易分解生成CuO、H2O和CO2,这三种生成物中共含有四种元素;
[实验探究](1)戒指的成分中有锌,故能和盐酸反应放出H2;实验室常用燃着的木条的方法检验这种可能含有的气体.
(2)碱式碳酸铜能和盐酸反应生成氯化铜,同时盐酸是过量的,故蓝色溶液中还含有CuCl2 、HCl等溶质;氯化铜和锌反应能置换出红色的铜,盐酸和锌反应放出氢气,所以可以观察到反应的现象是:①有气泡产生②有红色物质析出;
(3)锌和氯化亚铁反应生成铁和氯化锌,证明锌比铁活泼,又铁能置换氯化铜中的铜,所以可得出Cu<Fe<Zn;
故答案:
[查阅资料]
(1)4;
[实验探究]
(1)H2;燃着的木条,点燃;
(2)CuCl2;HCl(答案可互换);①有气泡产生;②有红色物质析出(溶液颜色变浅)(答案可互换)
(3)Cu<Fe<Zn;
点评 本题从物质的元素组成,物质的化学性质,如何分析溶液的成分,物质的检验,金属活动性顺序的应用,化学计算等方面进行考查,容量大,难易程度成阶梯上升,是一道很好的题.

练习册系列答案
 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
7.下列有关物质的分类错误的是( )
| A. | 生石灰属于氧化物 | B. | 小苏打属于盐 | ||
| C. | 酒精属于有机物 | D. | 干冰属于混合物 |
8.类推法是一种常见重要的学习方法,下列类推中错误的是( )
| A. | 铁、铜等很多金属难溶于水,铅是一种金属,铅可能也难溶于水 | |
| B. | 原子和分子均是微观粒子,在化学变化中原子不能再分,则分子也不能再分 | |
| C. | SO2与CO2一样,溶于水生成酸性物质,则SO2也能与NaOH溶液反应 | |
| D. | H2、CO、CH4气体燃烧前要进行验纯,其它可燃性气体不纯时也可能发生爆炸 |
5.携手“六城”同创,共建山青水绿、天蓝地净的美丽恩施.从化学的视角你认为下列不符合该主题的是( )
| A. | 绿化、亮化、美化环境 | B. | 必要时对私家车限行 | ||
| C. | 开发和利用新能源 | D. | 生活污水直排江河 |
12.下列对初中化学知识的总结,错误的是( )
| A. | 化学基本反应类型包括化合反应、分解反应、置换反应和复分解反应四种 | |
| B. | 六大基本营养素是蛋白质、糖类、油脂、维生素、无机盐和水 | |
| C. | 由同种元素组成的物质一定是纯净物 | |
| D. | 遇到火灾时,用湿毛巾捂住口鼻,匍匐逃离火灾现场 |
6.某兴趣小组对“铁锈(Fe2O3)与盐酸反应快慢的影响因素”进行了探究.
【提出问题】铁锈与盐酸反应的快慢受哪些因速的影响呢?
【猜想与假设】a.可能与盐酸的质量分数有关;
b.可能与反应的温度有关.
【设计实验】用相同质量的铁锈和足量的盐酸进行如表实验.
(1)写出铁锈与盐酸反应的化学方程式Fe2O3+6HCl═2FeCl3+3H2O.
(2)要比较温度对反应快慢的影响,应选择的实验编号是②③.
【得出结论】(3)从以上实验中可得出的结论是①温度越高,反应时间越短,反应速率越快;②酸的溶质质量分数越大,反应速率越快.
【实验拓展】(4)随后在铁锈与盐酸反应的试管中加入少量硫酸,发现反应明显加快,可能是硫酸中H+(填化学符号)加快了反应的速率,请设计一个合理的实验来验证你的假设在铁锈与盐酸反应的试管中加入少量硫酸钠溶液,发现反应速率没有改变,说明不是其中的硫酸根离子所起的作用.
(5)铁锈与盐酸反应的快慢可能还受哪些因速影响?设计实验验证.
【提出问题】铁锈与盐酸反应的快慢受哪些因速的影响呢?
【猜想与假设】a.可能与盐酸的质量分数有关;
b.可能与反应的温度有关.
【设计实验】用相同质量的铁锈和足量的盐酸进行如表实验.
| 实验编号 | 盐酸的质量分数 | 反应的速度 | 铁锈消失的时间 |
| ① | 6% | 20℃ | 240 s |
| ② | 10% | 20℃ | 115 s |
| ③ | 10% | 30℃ | 75 s |
(2)要比较温度对反应快慢的影响,应选择的实验编号是②③.
【得出结论】(3)从以上实验中可得出的结论是①温度越高,反应时间越短,反应速率越快;②酸的溶质质量分数越大,反应速率越快.
【实验拓展】(4)随后在铁锈与盐酸反应的试管中加入少量硫酸,发现反应明显加快,可能是硫酸中H+(填化学符号)加快了反应的速率,请设计一个合理的实验来验证你的假设在铁锈与盐酸反应的试管中加入少量硫酸钠溶液,发现反应速率没有改变,说明不是其中的硫酸根离子所起的作用.
(5)铁锈与盐酸反应的快慢可能还受哪些因速影响?设计实验验证.
10.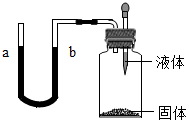 用如图所示的密闭实验装置,当胶头滴管内的液体滴下与固体接触时,液面a比液b高,但过一段时间U型管内的液面又回到持平的一组固体和液体组合是( )
用如图所示的密闭实验装置,当胶头滴管内的液体滴下与固体接触时,液面a比液b高,但过一段时间U型管内的液面又回到持平的一组固体和液体组合是( )
 用如图所示的密闭实验装置,当胶头滴管内的液体滴下与固体接触时,液面a比液b高,但过一段时间U型管内的液面又回到持平的一组固体和液体组合是( )
用如图所示的密闭实验装置,当胶头滴管内的液体滴下与固体接触时,液面a比液b高,但过一段时间U型管内的液面又回到持平的一组固体和液体组合是( )| A. | 食盐和水 | B. | 石灰石和稀盐酸 | ||
| C. | 固体氢氧化钠和水 | D. | 硝酸铵和水 |
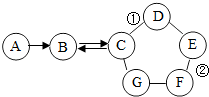 如图表示的是物质A~G相互间的关系“→”表示物质间存在的转化关系,“-”表示两端的物质能发生化学反应).相关信息如下:A、F都是单质,F是使用最多的金属材料,B是导致温室效应的主要气体之一,C在工业上广泛用于玻璃、造纸和洗涤剂的生产等,E是一种蓝色溶液.
如图表示的是物质A~G相互间的关系“→”表示物质间存在的转化关系,“-”表示两端的物质能发生化学反应).相关信息如下:A、F都是单质,F是使用最多的金属材料,B是导致温室效应的主要气体之一,C在工业上广泛用于玻璃、造纸和洗涤剂的生产等,E是一种蓝色溶液. 表示氮原子,
表示氮原子, 表示氧原子,
表示氧原子, 表示氢原子;各物质未配平).请分析在该反应中参加反应的NH3与O2的分子个数之比为4:5.
表示氢原子;各物质未配平).请分析在该反应中参加反应的NH3与O2的分子个数之比为4:5.