题目内容
5.氯化钠是一种可溶性重金属盐,广泛应用于化工领域.用毒重石(主要成分为BaCO3)制备氯化钡晶体工艺流程如图:
(1)本流程中“浓缩”、“结晶”属于物理变化.(选填“物理”或“化学”).
(2)滤液2中可利用的物质除水之外,还有BaCl2(填化学式).
(3)下列措施中,能提高原料的利用率和氯化钡晶体产量的有①②(选填序号).
①将滤液2通入到滤液1中 ②加入足量的稀盐酸.
分析 (1)根据物理变化和化学变化的判断依据进行分析;
(2)根据滤液2是氯化钡浓溶液结晶后得到的水溶液进行分析;
(3)根据题中的反应流程分析,哪个操作可以提高原理的利用率和氯化钡的产量,结合选项进行分析.
解答 解:(1)经过“浓缩”、“结晶”后,没有新物质生成,所以“浓缩”、“结晶”属于物理变化;
(2)滤液2是氯化钡浓溶液结晶后得到的水溶液,结晶后,晶体不会完全的析出,所以滤液2中可利用的物质除水之外,还有BaCl2;
(3)①将滤液2通入到滤液1中,滤液2中的氯化钡可以被重新的进行结晶,可以提高氯化钡晶体产量,故①正确;
②加入足量的稀盐酸,可以将碳酸钡完全反应,也可以能提高原料的利用率,故②正确.
故选:①②.
故答案为:(1)物理;
(2)BaCl2;
(3)①②.
点评 在解此类题时,首先分析题中的反应原理,然后将题中信息和课本知识的联系,看清每步操作的目的或反应实质即可较快解答.

练习册系列答案
相关题目
20.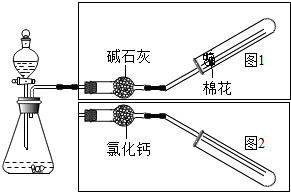 如图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是( )
如图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是( )
 如图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是( )
如图是实验室制取气体的装置,其中发生装置相同,干燥和集气装置有两套,分别用图1和图2表示.下列选项中正确的是( )| 发生装置中的药品 | 干燥和集气装置 | |
| A | 二氧化锰和双氧水 | 图1 |
| B | 大理石和稀盐酸 | 图2 |
| C | 锌和稀硫酸 | 图2 |
| D | 锌和稀盐酸 | 图1 |
| A. | A | B. | B | C. | C | D. | D |
10.日常生活中发生的下列变化属于化学变化的是( )
| A. | 玻璃破碎 | B. | 木材制成桌椅 | C. | 菜刀生锈 | D. | 湿衣服晾干 |
17.在空气中,与人类关系最密切的当属氧气.下列说法正确的是( )
| A. | 带火星的木条在氧气中能够复燃,说明氧气能支持燃烧 | |
| B. | 铁丝在氧气中剧烈燃烧,火星四射,说明氧气具有可燃性 | |
| C. | 氧气的化学性质非常活泼,能与所有的物质发生化学反应 | |
| D. | 用氯酸钾和二氧化锰制取氧气的反应不是分解反应 |
15.甲、乙、丙、丁四位同学在探究碱溶液与酚酞作用的实验时,发现了一个意外现象:
将酚酞试液滴入氢氧化钠溶液,溶液变成了红色,一会儿红色就消失了.这是什么原因呢?他们依据所学的科学知识,分别对这种意外现象的成因做了如下猜想:
甲:可能是酚酞变质的缘故;
乙:可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;
丙:可能是酚酞与空气中氧气反应,使红色消失的缘故;
丁:可能与氢氧化钠溶液质量分数大小有关,质量分数大的溶液中红色会消失.
(1)甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是若酚酞试剂变质,就不可能出现遇氢氧化钠溶液变红的现象.
丙同学认为乙同学的猜想也不正确,他的理由是生成的碳酸钠溶液显碱性,也可使酚酞试剂变红.
(2)为证实丙同学的猜想,还需作如下实验,请完成表.
(3)通过以上实验,四位同学看到:溶液先变成红色,一会儿红色又消失.因此酚酞红色褪去与氧气无关.若丁同学的猜想正确,设计如下实验证明并完成有关问题:
将酚酞试液滴入氢氧化钠溶液,溶液变成了红色,一会儿红色就消失了.这是什么原因呢?他们依据所学的科学知识,分别对这种意外现象的成因做了如下猜想:
甲:可能是酚酞变质的缘故;
乙:可能是氢氧化钠溶液与空气中二氧化碳反应的缘故;
丙:可能是酚酞与空气中氧气反应,使红色消失的缘故;
丁:可能与氢氧化钠溶液质量分数大小有关,质量分数大的溶液中红色会消失.
(1)甲同学刚提出自己的猜想,就遭到其余三位同学的否定,三位同学的理由是若酚酞试剂变质,就不可能出现遇氢氧化钠溶液变红的现象.
丙同学认为乙同学的猜想也不正确,他的理由是生成的碳酸钠溶液显碱性,也可使酚酞试剂变红.
(2)为证实丙同学的猜想,还需作如下实验,请完成表.
| 实验步骤 | 目的 |
| ①用煮沸过的蒸馏水配制氢氧化钠溶液. | 用煮沸过的蒸馏水:排出水中溶解的氧气 |
| ②在氢氧化钠溶液中滴入酚酞,并在上方滴一些植物油 | 滴一些植物油:隔绝空气 |
| 实验方法 | 预计观察到的现象 |
| 方案一:分别配制不同质量分数的氢氧化钠溶液,然后各滴加2滴酚酞试液. | 将滴有酚酞试液的质量分数大的氢氧化钠溶液加水稀释,溶液变红,说明与氢氧化钠溶液质量分数大小有关 |
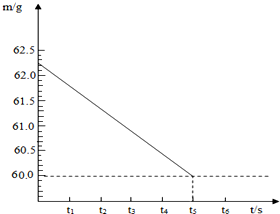 小红发现松软的面包、酥脆的饼干内部都有许多小孔(如图所示).为探究这个问题,她从面点师那里了解到:此类食品制作过程中加入膨松剂,碳酸氢钠就是一种常用的膨松剂.小红从超市买来一袋膨松剂(碳酸氢钠),按照研究物质的一般方法,对其进行探究.
小红发现松软的面包、酥脆的饼干内部都有许多小孔(如图所示).为探究这个问题,她从面点师那里了解到:此类食品制作过程中加入膨松剂,碳酸氢钠就是一种常用的膨松剂.小红从超市买来一袋膨松剂(碳酸氢钠),按照研究物质的一般方法,对其进行探究.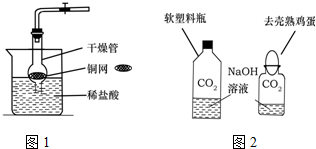 CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质:
CO2是初中化学重点研究的气体之一.某化学兴趣小组设计了如下实验来探究CO2的制取和性质: