题目内容
2.(1)在常见的铁、铝、铜三种金属中:①制造电线最好选用的金属是铜;②金属活动性最强的是铝;③请你写出与盐酸反应的一个化学方程式:2Al+6HCl=2AlCl3+3H2↑.(2)2014年8月江苏昆山发生铝粉尘爆炸.学生查阅资料:铝粉会与高温的水蒸气发生剧烈反应,生产氢氧化铝[Al(OH)3]和氢气,写出这样反应的化学方程式:2Al+H2O$\frac{\underline{\;高温\;}}{\;}$2Al(OH)3+H2↑.它是属于反应置换(填基本反应类型).请你对安全生产,防范粉尘爆炸提出合理化建议严禁烟火.
分析 根据已有的金属的性质以及金属活动性的顺序进行分析解答,根据反应物和生成物书写反应的化学方程式,根据特点判断反应类型,据此解答
解答 解:(1)在常见的铁、铝、铜三种金属中,铜的导电性最好,故制造电线最好选用的金属是铜;②这三种金属中,金属活动性最强的是铝;③铝能与盐酸发生反应生成氯化铝和氢气,故填:铜,铝,2Al+6HCl=2AlCl3+3H2↑;
(2)铝能与水高温反应生成氢氧化铝和氢气,该反应是一种单质和一种化合物反应生成另一种单质和另一种化合物属于置换反应,要防范粉尘爆炸,需要严禁烟火,故填:2Al+H2O$\frac{\underline{\;高温\;}}{\;}$2Al(OH)3+H2↑,置换,严禁烟火.
故答案为:(1)铜,铝,2Al+6HCl=2AlCl3+3H2↑;(2)2Al+H2O$\frac{\underline{\;高温\;}}{\;}$2Al(OH)3+H2↑,置换,严禁烟火.
点评 本题考查的是金属金属应用的知识,完成此题,可以依据已有的金属的性质进行.

练习册系列答案
相关题目
12.下列实验基本操作正确的是( )
| A. | 将实验剩余的药品及时放回原试剂瓶 | |
| B. | 将锌粒装入试管时,让锌粒缓缓地沿试管内壁滑到底部 | |
| C. | 给试管内的液体加热,液体的体积不超过试管容积的2/3 | |
| D. | 用酒精灯给试管内的物质加热,试管的底部与酒精灯灯芯接触 |

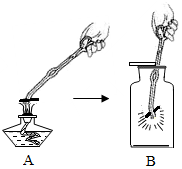 今年5月我市九年级学生进行了化学实验操作考试,考到了“木炭在氧气中燃烧”这一实验,如图所示,请回答:
今年5月我市九年级学生进行了化学实验操作考试,考到了“木炭在氧气中燃烧”这一实验,如图所示,请回答: 实验室用过氧化氢溶液在MnO2作催化剂的条件下制取氧气.分液漏斗可以通过活塞控制液体的滴加速度(如图)
实验室用过氧化氢溶液在MnO2作催化剂的条件下制取氧气.分液漏斗可以通过活塞控制液体的滴加速度(如图)