题目内容
4.下列关于资源、能源、环境等问题叙述错误的是( )| A. | 地球上的陆地淡水储量约占2.53%,但是可利用的淡水资源不足0.1% | |
| B. | 使化石燃料充分燃烧,既可以减少空气污染,又可以节约化石能源 | |
| C. | 可燃冰是乙醇水合物,外观像冰,具有能量高,燃烧值大等优点 | |
| D. | 石油分解后可得到汽油、煤油、柴油等一系列产品 |
分析 A、根据淡水资源不充足解答;
B、根据使燃料充分燃烧的优点进行分析判断;
C、根据可燃冰外观像冰主要含有甲烷水合物解答;
D、根据从石油里提炼柴油、汽油、煤油的过程叫石油分馏,属于物理变化解答.
解答 解:
A、地球上的陆地淡水储量约占2.53%,但是可供利用的淡水资源不足1%,正确;
B、使燃料充分燃烧,既可以减少空气污染,又可以节约化石能源,正确;
C、可燃冰外观像冰主要含有甲烷水合物,将成为未来的主要化石能源,正确;
D、从石油里提炼柴油、汽油、煤油的过程叫石油分馏,属于物理变化.因为它是根据不同的烯烃的沸点不同,然后蒸馏让它们分离开来. 而不是分解,分解属于化学变化.错误.
故选D.
点评 本题考查的是我们身边的资源、能源、环境和化学息息相关的一系列问题,是社会关注的焦点,关注社会热点,了解常见实际问题的解决方法,是解决问题的前提.

练习册系列答案
相关题目
15.欲配制100g质量分数为10%的氯化钠溶液,一定能用到的仪器组合是( )
①托盘天平 ②烧杯 ③玻璃棒 ④50ml量筒.
①托盘天平 ②烧杯 ③玻璃棒 ④50ml量筒.
| A. | ①② | B. | ①②③ | C. | ①②④ | D. | ①②③④ |
12.化学小组同学针对二氧化碳进行趣味实验:将燃烧的钠迅速伸入到盛有二氧化碳的集气瓶中,钠继续燃烧,冷却后瓶底附着黑色颗粒,瓶壁上附粘附着白色物质.
【提出问题】黑色颗粒和白色物质是什么?
【查阅资料】氧化钠为白色粉末,与与氧化钙的性质相似遇水能发生反应.
【做出猜想】甲认为生成的黑色颗粒是炭;白色物质可能是:①氧化钠、②碳酸钠、③氧化钠与碳酸钠的混合物.乙认为白色物质还可能是氢氧化钠或碳酸氢钠.甲认为乙的猜想是错误的,理由是反应物中无氢元素.
【实验探究】甲通过实验分析,确定黑色颗粒是炭,并对白色物质进行实验探究.
【反思评价】你认为方案1是否合理:不合理(填“合理”或“不合理”)
丙认为方案2得到的结论不正确,理由是碳酸钠在溶液中也显碱性.
【得出结论】钠在二氧化碳中燃烧的化学方程式为4Na+3CO2$\frac{\underline{\;点燃\;}}{\;}$2Na2CO3+C.
通过以上探究还能获得哪些结论:燃烧不一定要有氧气参加(写一条).
【提出问题】黑色颗粒和白色物质是什么?
【查阅资料】氧化钠为白色粉末,与与氧化钙的性质相似遇水能发生反应.
【做出猜想】甲认为生成的黑色颗粒是炭;白色物质可能是:①氧化钠、②碳酸钠、③氧化钠与碳酸钠的混合物.乙认为白色物质还可能是氢氧化钠或碳酸氢钠.甲认为乙的猜想是错误的,理由是反应物中无氢元素.
【实验探究】甲通过实验分析,确定黑色颗粒是炭,并对白色物质进行实验探究.
| 方案 | 实验操作 | 实验现象 | 结论 |
| 方案1 | 取样品少量于试管中,向其中加入足量的稀盐酸 | 产生气泡 | 白色物质是碳酸钠 |
| 方案2 | 取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入无色酚酞试液 | 溶液变成红色 | 白色物质为氧化钠 |
| 方案3 | ①取样品少量于试管中,加入适量水,振荡,样品全部溶于水,向其中加入过量的氯化钙溶液 | 出现白色沉淀 | 白色物质是碳酸钠 |
| ②静置片刻,取上层清液于试管中,滴加酚酞(或硫酸铜)(要求:所填试剂属于不同类别) | 无明显现象 |
丙认为方案2得到的结论不正确,理由是碳酸钠在溶液中也显碱性.
【得出结论】钠在二氧化碳中燃烧的化学方程式为4Na+3CO2$\frac{\underline{\;点燃\;}}{\;}$2Na2CO3+C.
通过以上探究还能获得哪些结论:燃烧不一定要有氧气参加(写一条).
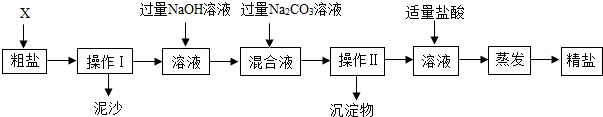
16.传统腌制松花蛋的主要配料是氧化钙、纯碱和食盐.某活动小组将这三种物质混合后加入适量水搅拌、过滤后,对滤液中溶质的成分进行探究:
(1)【猜想与假设】
甲同学猜想:可能是NaCl、Ca(OH)2、Na2CO3
乙同学猜想:可能是NaCl、NaOH、Na2CO3
丙同学猜想:可能是NaCl、Ca(OH)2、NaOH
丁同学猜想:可能是NaCl、NaOH
【交流与评价】大家一致认为甲同学的猜想不成立,理由一是:Ca(OH)2和Na2CO3能反应而不能共存,理由二是:没有氢氧化钙和碳酸钠反应生成的氢氧化钠
(2)【活动与探究】
(3)【解释与结论】丁同学的结论是否正确不正确.丁同学和乙同学使用了相同的试剂,却没有看到气泡产生,你认为可能的原因是:少量的盐酸只能够和氢氧化钠反应生成碳酸钠和水.
(1)【猜想与假设】
甲同学猜想:可能是NaCl、Ca(OH)2、Na2CO3
乙同学猜想:可能是NaCl、NaOH、Na2CO3
丙同学猜想:可能是NaCl、Ca(OH)2、NaOH
丁同学猜想:可能是NaCl、NaOH
【交流与评价】大家一致认为甲同学的猜想不成立,理由一是:Ca(OH)2和Na2CO3能反应而不能共存,理由二是:没有氢氧化钙和碳酸钠反应生成的氢氧化钠
(2)【活动与探究】
| 实验步骤 | 实验现象及相关化学方程式 | 实验结论 |
| 乙同学取一定量的滤液于试管中,向其中加入一定量的盐酸 | 有大量气泡生成,写出产生气泡的化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑ | 乙同学的猜想成立 |
丙同学取一定量的滤液于试管中,向其中加入一定量的碳酸钠溶液 | 实验现象产生白色沉淀 | 丙同学的猜想成立 |
| 丁同学取一定量的滤液于试管中,向其中滴加少量盐酸. | 无气泡产生 | 乙同学猜想不成立 |
14.下列物质的性质与所对应的用途没有直接关系的是( )
| A. | 氧气的密度比空气略大--用于急救病人 | |
| B. | 氮气的性质稳定--作焊接保护气 | |
| C. | 稀有气体通电发光--制作电光源 | |
| D. | 干冰升华吸热--用于人工降雨 |
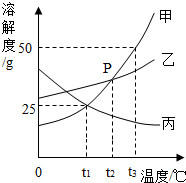 如图是甲、乙、丙三种固体物质的溶解度曲线,请根据溶解度曲线回答下列问题:
如图是甲、乙、丙三种固体物质的溶解度曲线,请根据溶解度曲线回答下列问题: