题目内容
15.某粗盐提纯后得到的“精盐”中还含有少量可溶性杂质CaCl2、MgCl2.小青同学设计了如图所示实验方案来除去可溶性杂质.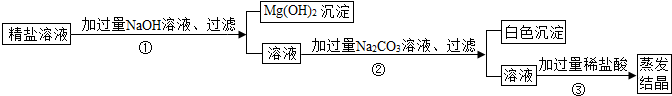
(1)步骤①中,NaOH为何要加入过量?除去全部的氯化镁.
(2)步骤②中得到的白色沉淀是CaCO3(填化学式).
(3)步骤③中加稀盐酸是为了除去溶液中的CD.
A.CaCl2 B.MgCl2 C.NaOH D.Na2C03.
分析 除钙离子用碳酸根,除镁离子用氢氧根,因为加入的试剂都是过量的,所以后加的试剂要把先加的试剂所带入的杂质除掉,加入过量的稀盐酸,这样可以除去多余的碳酸根离子和氢氧根离子.
解答 解:(1)本实验的过程为①加过量NaOH溶液,与MgCl2发生反应,生成Mg(OH)2沉淀和氯化钠,所以步骤①中,加入过量NaOH的目的是除去全部的氯化镁;
(2)加过量Na2CO3溶液,与CaCl2发生反应,生成CaCO3沉淀和氯化钠,所以步骤②中得到的白色沉淀是碳酸钙;
(3)加适量盐酸,与①中过量NaOH溶液和②中过量Na2CO3溶液发生反应,生成氯化钠、水和二氧化碳气体,步骤③中加稀盐酸是为了除去溶液中的氢氧化钠和碳酸钠.
故答案为:
(1)除去全部的氯化镁;
(2)CaCO3;
(3)CD.
点评 通过离子间的反应把离子转化为沉淀和气体除去,但要注意加入试剂的量,最后不能带入新的杂质.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
6.下列化学用语表达正确的是( )
| A. | 两个氮原子:N2 | B. | 三个氢分子3H2 | C. | 钙离子:Ca+2 | D. | 硫酸亚铁:FeSO4 |
3.物质在不断运动变化着,属于物理变化的是( )
| A. | 鸡蛋清中加入硫酸铜溶液“凝固” | |
| B. | 打开浓盐酸瓶口“冒白雾” | |
| C. | 全毛绒线放入氢氧化钠溶液中“溶解” | |
| D. | 氢氧化钠溶液中滴入酚酞“变化” |
20.下列物质鉴别的方法错误的是( )
| A. | 区别二氧化碳、氧气和空气--分别将燃着的木条伸入瓶中,观察现象 | |
| B. | 区别过氧化氢和蒸馏水--加入MnO2,看是否有气泡 | |
| C. | 区别硬水与软水--常用肥皂水检验,泡沫减少产生浮渣的是硬水 | |
| D. | 区别二氧化锰和氧化铜--观察颜色 |
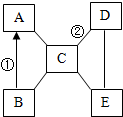 A、B、C、D、E是初中化学常见的五种不同类别的物质,其中B为红色固体,C是胃液的主要成分,E俗称苏打.图中“-”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去.请回答下列问题:
A、B、C、D、E是初中化学常见的五种不同类别的物质,其中B为红色固体,C是胃液的主要成分,E俗称苏打.图中“-”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去.请回答下列问题: 如图表示几种化合物能通过一步反应转化为含镁化合物M
如图表示几种化合物能通过一步反应转化为含镁化合物M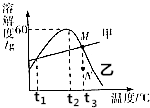 如图是甲、乙两种化合物的溶解度曲线示意图,据此得到的结论正确的是C.
如图是甲、乙两种化合物的溶解度曲线示意图,据此得到的结论正确的是C.