题目内容
5.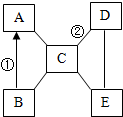 A、B、C、D、E是初中化学常见的五种不同类别的物质,其中B为红色固体,C是胃液的主要成分,E俗称苏打.图中“-”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去.请回答下列问题:
A、B、C、D、E是初中化学常见的五种不同类别的物质,其中B为红色固体,C是胃液的主要成分,E俗称苏打.图中“-”表示两端的物质间能发生化学反应,“→”表示物质间存在转化关系,部分反应物、生成物及反应条件已略去.请回答下列问题:(1)写出下列物质的化学式:AFe;ENa2CO3.
(2)写出①、②反应的化学方程式:①3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;②Ca(OH)2+2HCl=CaCl2+2H2O.
(3)C与E反应的基本反应类型为复分解反应.
分析 根据A、B、C、D、E是初中化学常见的五种不同类别的物质,C是胃液的主要成分,所以C是盐酸,B为红色固体,B和盐酸会发生反应,所以B是氧化铁,氧化铁会转化成A,A和盐酸会发生反应,所以A是铁,E广泛用于玻璃、造纸、纺织和洗涤剂的生产等,E和盐酸会发生反应,所以E是碳酸钠,D和盐酸、碳酸钠会反应,所以D是碱,D可以是氢氧化钙,然后将推出的各种物质代入转化关系中验证即可.
解答 解:(1)A、B、C、D、E是初中化学常见的五种不同类别的物质,C是胃液的主要成分,所以C是盐酸,B为红色固体,B和盐酸会发生反应,所以B是氧化铁,氧化铁会转化成A,A和盐酸会发生反应,所以A是铁,E广泛用于玻璃、造纸、纺织和洗涤剂的生产等,E和盐酸会发生反应,所以E是碳酸钠,D和盐酸、碳酸钠会反应,所以D是碱,D可以是氢氧化钙,经过验证,推出的各种物质均满足题意,推导正确,所以A是Fe,E是Na2CO3;
(2)反应①是氧化铁和一氧化碳在高温的条件下反应生成铁和二氧化碳,化学方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
反应②是氢氧化钙和盐酸反应生成氯化钙和水,化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O;
(3)C与E的反应是盐酸和碳酸钠反应生成氯化钠和水及二氧化碳,满足复分解反应的条件,所以该反应属于复分解反应.
故答案为:
(1)Fe,Na2CO3;
(2)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;Ca(OH)2+2HCl=CaCl2+2H2O;
(3)复分解反应.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

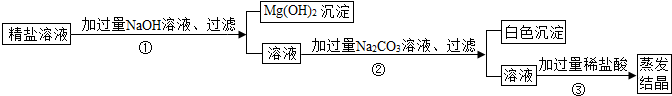
【提出问题】这瓶试剂可能是什么溶液呢?
【查阅资料】碱性的Na2CO3溶液与中性的CaCl2溶液能发生反应.
【作出猜想】(1)可能是NaOH溶液;(2)可能是Na2CO3溶液;(3)可能是NaCl溶液.
【设计并实验】
| 实验 | 实验操作 | 主要实验现象 | 实验结论和解释 |
| Ⅰ | 取样于试管中,向其中滴加几滴无色酚酞溶液. | 无色溶液变红色 | 该溶液不可能是NaCl溶液. |
| Ⅱ | 另取样于另一支试管中,向其中滴加足量的稀盐酸. | 产生大量的气泡 | 该溶液中为碳酸钠.有关反应的化学方程式为:Na2CO3+2HCl=2NaCl+H2O+CO2↑. |
老师提示,不需另取样,只要在实验Ⅰ后的试管中加入足量CaCl2溶液,若观察到产生白色沉淀,且溶液红色不褪去现象,即可说明该溶液中有氢氧化钠.
| A. | NaCl | B. | NaHCO3 | C. | Na2CO3 | D. | NaOH |
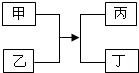
| A. | 若甲、丁为单质,则该反应一定是置换反应 | |
| B. | 若丙为气体,则甲、乙中一定有单质 | |
| C. | 若丁为水,则该反应一定是复分解反应 | |
| D. | 若丙为沉淀,则甲、乙中一定有一种物质是碱 |
| A. | 氯化钠 | B. | 金刚石 | C. | C60 | D. | 氯化氢 |
| A. | 拒绝使用一次性筷子或纸杯等用品 | B. | 爱护一草一木 | ||
| C. | 取超市购物时自带环保购物袋 | D. | 电脑长期待机 |