题目内容
7. 水是人类宝贵的自然资源.
水是人类宝贵的自然资源.(1)天然水中含有许多杂质,实验室用过滤装置除去水中不溶性杂质,需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和玻璃棒(填玻璃仪器).
(2)生活中常用肥皂水来区分硬水和软水.
(3)氯气可用作自来水的消毒剂,实验室制取氯气的化学方程式为:
MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$X+Cl2↑+2H2O,X的化学式为MnCl2.
(4)天然降水中会溶解部分空气里的CO2气体,因此正常雨水的pH≈5.6.
(5)甲和乙两种固体物质的溶解度曲线如图所示.
①t1℃时,甲和乙的溶解度相等(填“相等”或“不相等”).
②t2℃时,若甲和乙的饱和溶液各100g,则两种溶液中溶剂的质量大小关系为:甲<乙(填“>”、“=”或“<”).
③t2℃时,150g甲的饱和溶液中溶质的质量分数为33.3%(计算结果精确到0.1%).
分析 (1)过滤操作,过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和玻璃棒;
(2)区分硬水和软水的方法是:用肥皂水,加入肥皂水,泡沫多的是软水,泡沫少的是硬水;
(3)质量守恒定律,等号两边各原子的种类和数目相等;
(4)二氧化碳和水反应;
(5)根据题目信息和溶解度曲线可知:甲、乙两种固体物质的溶解度,都是随温度升高而增大,而甲的溶解度随温度的升高变化比乙大;有关质量分数的计算要准确;
解答 解:(1)过滤需要用到的仪器有带铁圈的铁架台、烧杯、漏斗和玻璃棒;故答案为:玻璃棒;
(2)区分硬水和软水的方法是:用肥皂水,加入肥皂水,泡沫多的是软水,泡沫少的是硬水;故答案为:肥皂水;
(3)根据质量守恒定律,等号两边各原子的种类和数目相等,在MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$X+Cl2↑+2H2O,X是二氯化锰,故答案为:MnCl2;
(4)天然降水中会溶解部分空气里的二氧化碳,因此正常雨水的pH≈5.6,因为二氧化碳和水反应生成碳酸,故答案为:CO2;
(5)t1℃时,甲和乙的溶解度相等,因为他们在该温度下有交点;t2℃时,若甲和乙的饱和溶液各100g,则两种溶液中溶剂的质量大小关系为:甲小于乙,因为在该温度下甲的溶解度大于乙;t2℃时,150g甲的饱和溶液中溶质的质量分数=$\frac{50g}{150g}×100%$≈33.3%;故答案为:①相等 ②<③33.3%;
点评 本考点考查了过滤、硬水与软水的区分、质量守恒定律、溶解度曲线及其应用,通过溶解度曲线我们可以获得很多信息;还考查了有关溶液和溶质质量分数的计算,有关的计算要准确,本考点主要出现在选择题和填空题中.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
17.正确的实验操作是进行科学实验的重要保障.下列操作中,合理的是( )
| A. | 少量酒精在实验台上燃烧时,立即用湿抹布盖灭 | |
| B. | 稀释浓硫酸时,将水注入盛有浓硫酸的烧杯中 | |
| C. | 测定某溶液的pH时,先用水将pH试纸润湿 | |
| D. | 向试管中滴加液体时,将胶头滴管伸入试管内,防止液体溅出 |
15.下列物质使用过程中发生化学变化的是( )
| A. |  纺织布匹 | B. |  用玻璃刀切割玻璃 | ||
| C. |  燃放烟花爆竹 | D. |  用干冰进行人工降雨 |
12.通过下列图示实验得出的结论中正确的是( )

| A. | 图1所示实验既说明空气中氧气约占空气体积的$\frac{1}{5}$,又说明氮气不易溶于水 | |
| B. | 图2所示实验既说明电解水生成氢气和氧气,又说明水是由氢气和氧气组成的 | |
| C. | 图3所示实验既可探究可燃物的燃烧条件,又说明白磷能与水反应 | |
| D. | 图4所示实验既可探究铁生锈需要与氧气接触的条件,又说明铁生锈需要与水接触的条件 |
19.下列化学知识的总结或应用,完全正确的一组是( )
| A | 误食重金属盐立即饮用牛奶、豆浆 米、面、土豆主要为人体补充油脂 | B | 在化粪池、加油站附近燃放烟花炮竹 在室内烧炭取暖时一定要安装烟囱 |
| C | 用活性炭除去水中的异味和色素 用灼热Fe2O3除去CO2中混有的CO | D | 陶瓷、聚乙烯、涤纶属于有机合成材料 钢筋混凝土、机动车轮胎属于复合材料 |
| A. | A | B. | B | C. | C | D. | D |
17.下列课外实验中,不能达到实验目的是( )
| A. | 用冷碟子收集蜡烛火焰上方,制取炭黑 | |
| B. | 用洁净的鸡蛋壳加入食醋,制取二氧化碳 | |
| C. | 用10%的氯化钠溶液浸泡新鲜的树叶,制作叶脉书签 | |
| D. | 用报纸和保鲜膜分别蒙住盛等体积水的两只相同的烧杯,比较报纸和保鲜膜的透气性 |
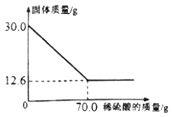 菱铁矿(主要成分是FeCO3)是炼铁的原料,现取30.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图所示.
菱铁矿(主要成分是FeCO3)是炼铁的原料,现取30.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图所示.