题目内容
(1)某校课外活动小组在学习了2Cu+O2 2CuO这一性质后,对空气中氧气含量的测定实验做了如下改进:
2CuO这一性质后,对空气中氧气含量的测定实验做了如下改进:
在由两个注射器组成的密闭系统内有20mL空气(如下图所示).然后给装有铜丝的玻璃管加热,同时交替缓慢推动两个注射器的活塞,至玻璃管内的铜丝变黑且较长时间内无进一步变化.停止加热后,待冷却至室温将气体全部推至一个注射器中.

请根据你对上述实验的理解回答下面的问题:
①实验结束后,注射器内空气的体积约减少了______,这是因为______;
②在实验的加热过程中,交替缓慢推动两注射器的目的是______;
③改进后的实验只是粗略测定空气中氧气含量的一种方法,你认为造成该实验不够精确的可能原因有:
A______
B______.
(2)根据你目前所具备的知识,以金属锌、氧化铜和稀硫酸三种物质为原料,设计出两种可在实验室实施的制备金属铜的实验方案(不必写化学方程式只写出简单过程即可):
方案一:______;
方案二:______;
两种方案相比较,你认为哪一个方案更好?请说明理由.______.
解:(1)由于铜的氧化反应只消耗掉了空气中的氧气,而氧气在空气中约占空气体积的 15,可得出答案:50×15=10ml,故答案为:①10;氧气的体积约占空气总体积的 15,注射器中的氧气被铜消耗掉了;②交替缓慢推动两个注射器的目的是使封闭空间的氧气与铜网充分接触,使空气中的氧气与铜网充分反应.③交替缓慢推动两个注射器的目的是使封闭空间的氧气充分反应,但是推动的缓慢程度不易控制,易得出实验不精确的地方可能是因为空气中的氧气没有完全被铜网消耗掉.
故答案为:(1)① ,空气中的氧气与铜反应,被消耗掉了;
,空气中的氧气与铜反应,被消耗掉了;
②使空气中的氧气充分与铜发生反应;
③A.两注射器之间的玻璃管中可能预先留有空气;B.铜丝未能完全反应掉空气中的氧气.
(2)方案主要是从利用氢气还原氧化铜和先转化成盐在利用金属进行置换制的,选择方案是主要是考虑节约能源,操作方便为出发点.
故答案为:方案一:Zn H2
H2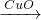 Cu;方案二:Cu
Cu;方案二:Cu CuSO4
CuSO4 Cu
Cu
方案二较好.因方案二不需加热、装置简单,操作方便,原料利用率高
分析:(1)①铜丝与空气中的氧充分反应,消耗掉空气中氧气,由空气中氧气的体积比容易求出空气减少的体积.
②由实验条件可推出交替缓慢推动两个注射器的目的是使封闭空间的氧气充分反应.
③交替缓慢推动两个注射器的目的是使封闭空间的氧气充分反应,但是推动的缓慢程度不易控制,易得出实验不精确的地方.
(2)利用所给的物质主要是考虑两个方面的问题,一是制取氢气并还原氧化铜,而是转化成盐后利用金属与盐溶液的反应制取出铜.
点评:本题能通过实验探究的方式考查了铜与氧气的反应,空气中氧的体积分数、有关铜的制取方式的选择,提高了学生学以致用的意识.
故答案为:(1)①
 ,空气中的氧气与铜反应,被消耗掉了;
,空气中的氧气与铜反应,被消耗掉了;②使空气中的氧气充分与铜发生反应;
③A.两注射器之间的玻璃管中可能预先留有空气;B.铜丝未能完全反应掉空气中的氧气.
(2)方案主要是从利用氢气还原氧化铜和先转化成盐在利用金属进行置换制的,选择方案是主要是考虑节约能源,操作方便为出发点.
故答案为:方案一:Zn
 H2
H2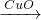 Cu;方案二:Cu
Cu;方案二:Cu CuSO4
CuSO4 Cu
Cu方案二较好.因方案二不需加热、装置简单,操作方便,原料利用率高
分析:(1)①铜丝与空气中的氧充分反应,消耗掉空气中氧气,由空气中氧气的体积比容易求出空气减少的体积.
②由实验条件可推出交替缓慢推动两个注射器的目的是使封闭空间的氧气充分反应.
③交替缓慢推动两个注射器的目的是使封闭空间的氧气充分反应,但是推动的缓慢程度不易控制,易得出实验不精确的地方.
(2)利用所给的物质主要是考虑两个方面的问题,一是制取氢气并还原氧化铜,而是转化成盐后利用金属与盐溶液的反应制取出铜.
点评:本题能通过实验探究的方式考查了铜与氧气的反应,空气中氧的体积分数、有关铜的制取方式的选择,提高了学生学以致用的意识.

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
某校化学课外活动小组在一次活动中,取刚降到地面的雨水水样,每隔5分钟用pH计测定一次pH,其数据如下表:
| 测定时刻 | 6:05 | 6:10 | 6:15 | 6:20 | 6:25 | 6:30 |
| pH | 4.95 | 4.94 | 4.94 | 4.88 | 4.86 | 4.85 |
(1)所取的雨水是否为酸雨?________(填“是”或“否”);在测定的期间,雨水水样的酸性随着时间的变化逐渐________(填“增强”或“减弱”).
(2)小乐改用pH试纸测定雨水的酸碱度,他先将PH试纸润湿,再用玻璃棒蘸取待测雨水滴到PH试纸上,立即与标准比色卡对比读数,此时他测得的PH值应会________(填“偏大”“偏小”“不变”).
(3)为了改善城市环境质量,下列措施能减少酸雨的是________(填序号):
①推广清洁能源
②减少用煤直接作燃料
③淘汰尾气不达标的汽车
④限制燃放烟花爆竹⑤限制并有偿使用塑料袋.



