题目内容
8.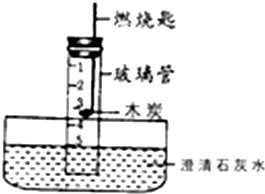 如右图进行测定空气中氧气含量实验(玻璃管分为6等分,实验前液面停留在管内5刻度处).
如右图进行测定空气中氧气含量实验(玻璃管分为6等分,实验前液面停留在管内5刻度处).(1)澄清石灰水的作用有③(填序号).
①加快降温 ②吸收有毒生成物,防止污染空气 ③吸收CO2,保证实验成功
(2)实验结束后,玻璃管内液体增加了25mL,玻璃管总容积为150mL,
(3)所取木炭粉的质量理论上最少是多少克?(提示:①3g木炭粉燃烧需消耗8g氧气 ②氧气密度为1.4g/L.③计算结果保留两位小数)
分析 (1)木炭燃烧产生了二氧化碳,而二氧化碳为气体,为了使实验准确,所以用澄清石灰水保证实验成功,可以据此解答该题;
(2)氧气约占空气体积的五分之一,可以据此判断玻璃管的总容积;
(3)根据题中的提示结合密度公式来完成该题的解答.
解答 解:(1)木炭燃烧产生了二氧化碳,而二氧化碳为气体,为了使实验准确,所以用澄清石灰水保证实验成功,故选③;
(2)氧气约占空气体积的五分之一,所以玻璃管的总容积为:25mL÷$\frac{1}{6}$=150mL;
(3)根据题意可以知道消耗的氧气的体积为25mL,即消耗的氧气的质量为:0.025L×1.4g/L=0.035g
3g木炭粉能够消耗8g氧气,所以消耗0.035g氧气需要木炭粉的质量为:0.035g×$\frac{3}{8}$≈0.01g.
答:所取木炭粉的质量理论上最少是0.01克.
故答案为:(1)③;
(2)150;
(3)0.01g.
点评 空气是人类宝贵的自然资源,在中考中占有重要的地位,特别是空气中氧气含量的测定,要注意测定原理、实验关键、现象和结论、装置的评价和改进等内容的考查.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
19.学习了化学肥料后,小凯同学在家中将氯化铵与生石灰和水放在不锈钢杯子中用筷子搅拌混合,问到了一股刺激性气味的气体,他对这种气体产生了好奇,于是进行了以下探究:
【提出猜想】产生的气体是:
猜想1:氯化铵
猜想2:氧气
猜想3:氨气(NH3)
猜想4:二氧化硫
小芬同学认为猜想2不正确,原因是氧气无色无味;小强同学认为猜想4也不正确,原因是氯化铵与生石灰和水只有氮、氢、氯、钙、氧元素,二氧化硫中含有硫元素.
【设计实验】为了确定该气体,小凯同学设计了以下方案进行验证,请完成下表
【反思与评价】
(1)以上实验中,pH试纸不需要用蒸馏水湿润也能证明气体是氨气,理由是生石灰和水反应放出大量的热,水受热产生较多的水蒸气,可以将pH试纸湿润.
(2)实验小组同学把做完实验的pH试纸放在洁净的玻璃片上,过了一会儿,发现试纸是湿的,但颜色发生了改变,pH变成了7左右,你认为可能的原因是由于氨水极易挥发,氨气挥发掉了,pH变成了7左右.
【提出猜想】产生的气体是:
猜想1:氯化铵
猜想2:氧气
猜想3:氨气(NH3)
猜想4:二氧化硫
小芬同学认为猜想2不正确,原因是氧气无色无味;小强同学认为猜想4也不正确,原因是氯化铵与生石灰和水只有氮、氢、氯、钙、氧元素,二氧化硫中含有硫元素.
【设计实验】为了确定该气体,小凯同学设计了以下方案进行验证,请完成下表
| 实验步骤 | 实验现象 | 实验结论 |
| 将氯化铵与生石灰和水放在不锈钢的杯子中用筷子搅拌混合后,在杯口放一片湿润的红色石蕊试纸 | 产生刺激性气味的气体,湿润的红色石蕊试纸变蓝 | 猜想3正确.反应的化学方程式为CaO+H2O═Ca(OH)2和2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑ |
(1)以上实验中,pH试纸不需要用蒸馏水湿润也能证明气体是氨气,理由是生石灰和水反应放出大量的热,水受热产生较多的水蒸气,可以将pH试纸湿润.
(2)实验小组同学把做完实验的pH试纸放在洁净的玻璃片上,过了一会儿,发现试纸是湿的,但颜色发生了改变,pH变成了7左右,你认为可能的原因是由于氨水极易挥发,氨气挥发掉了,pH变成了7左右.
16.工业酒精中含有甲醇,关于甲醇的下列叙述正确的是( )


| A. | 甲醇是由多原子构成的 | |
| B. | 甲醇中氧、碳、氢原子的个数比为1:4:1 | |
| C. | 甲醇中含有18个电子 | |
| D. | 一个甲醇分子中有6个原子核 |

 如图为某学生设计的用高锰酸钾制取氧气的装置图,按要求回答:
如图为某学生设计的用高锰酸钾制取氧气的装置图,按要求回答: