题目内容
19.学习了化学肥料后,小凯同学在家中将氯化铵与生石灰和水放在不锈钢杯子中用筷子搅拌混合,问到了一股刺激性气味的气体,他对这种气体产生了好奇,于是进行了以下探究:【提出猜想】产生的气体是:
猜想1:氯化铵
猜想2:氧气
猜想3:氨气(NH3)
猜想4:二氧化硫
小芬同学认为猜想2不正确,原因是氧气无色无味;小强同学认为猜想4也不正确,原因是氯化铵与生石灰和水只有氮、氢、氯、钙、氧元素,二氧化硫中含有硫元素.
【设计实验】为了确定该气体,小凯同学设计了以下方案进行验证,请完成下表
| 实验步骤 | 实验现象 | 实验结论 |
| 将氯化铵与生石灰和水放在不锈钢的杯子中用筷子搅拌混合后,在杯口放一片湿润的红色石蕊试纸 | 产生刺激性气味的气体,湿润的红色石蕊试纸变蓝 | 猜想3正确.反应的化学方程式为CaO+H2O═Ca(OH)2和2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑ |
(1)以上实验中,pH试纸不需要用蒸馏水湿润也能证明气体是氨气,理由是生石灰和水反应放出大量的热,水受热产生较多的水蒸气,可以将pH试纸湿润.
(2)实验小组同学把做完实验的pH试纸放在洁净的玻璃片上,过了一会儿,发现试纸是湿的,但颜色发生了改变,pH变成了7左右,你认为可能的原因是由于氨水极易挥发,氨气挥发掉了,pH变成了7左右.
分析 【提出猜想】根据气体的性质和质量守恒定律分析;
【设计实验】根据铵盐与碱性物质混合研磨后能放出有刺激性气味的气体氨气,氨气能使湿润的红色石蕊试纸变蓝色,进行分析判断;
【反思与评价】(1)根据反应的产物分析;(2)根据氨水的挥发性分析.
解答 解:【提出猜想】氧气无色无味,而小凯闻到了一股刺激性气味的气体,故猜想2不正确,由质量守恒定律可知反应前后元素的种类不变,氯化铵与生石灰和水只有氮、氢、氯、钙、氧元素,二氧化硫中含有硫元素,故猜想4也不正确;
【设计实验】由题意,将氯化铵与生石灰和水混合后,用湿润的红色石蕊试纸放在试管口,湿润红色石蕊试纸会变蓝色,这是检验铵盐的方法,产生的气体是氨气,该实验说明铵盐能和碱反应放出氨气.反应的方程式为:CaO+H2O═Ca(OH)2和2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑.
【反思与评价】(1)由于反应中生石灰和水反应放出大量的热,水受热产生较多的水蒸气,可以将pH试纸湿润;
(2)由于氨水极易挥发,把做完实验的pH试纸放在洁净的玻璃片上,过了一会儿,氨气挥发掉了,pH变成了7左右.
故答案为:【提出猜想】氧气无色无味;氯化铵与生石灰和水只有氮、氢、氯、钙、氧元素,二氧化硫中含有硫元素;
【设计实验】3;2NH4Cl+Ca(OH)2=CaCl2+2H2O+2NH3↑.
【反思与评价】(1)生石灰和水反应放出大量的热,水受热产生较多的水蒸气,可以将pH试纸湿润;
(2)由于氨水极易挥发,氨气挥发掉了,pH变成了7左右.
点评 本考点属于实验探究题,还考查了化学方程式的书写.实验探究题是近几年中考的热点之一,它包括实验方法和过程的探究,实验结论和实验规律的探究等.本题通过实验资料和实验分析,得到了正确的结论,属于结论性探究.同学们要具体分析,综合掌握.本考点主要出现在实验题中.

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案| A. | 石墨 生石灰 酒精 | B. | 稀有气体 二氧化碳 稀硫酸 | ||
| C. | 氧气 干冰 大理石 | D. | 生铁 水 生石灰 |
| A. | 用加热煮沸的方法将海水淡化 | |
| B. | 为了增加养鱼池中氧气的溶解度,人们会在鱼池中设立水泵,把水洒向空中 | |
| C. | 用二氧化碳灭火器扑灭图书、档案等物的失火,因为它流动性好,喷射率高 | |
| D. | 发生火灾时可用湿毛巾捂住口鼻.低下身子沿墙壁跑出火灾区 |
| A. | 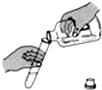 倾倒液体 | B. |  检查气密性 | ||
| C. | 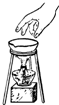 移走加热的蒸发皿 | D. |  闻气体的气味 |
| A. | 粉刷墙壁用的乳胶漆是乳浊液 | |
| B. | 宽阔的柏油路面所用的沥青是煤炼制的产品 | |
| C. | 改造时用的铝制门窗不用进行防锈处理 | |
| D. | 大理石围栏主要成分是碳酸钙 |
| 名称 | 4个铁原子 | 在氧化钠中,钠元素显正一价 | 2个氮气 分子 | 3个二氧化硫 分子 | 5个硝酸根 离子 | +6价的硫元素 | 由Fe3+和OH- 构成的氢氧化铁 |
| 化学 符号 | 4Fe | $\stackrel{+1}{Na}$2O | 2N2 | 3SO2 | 5NO3- | $\stackrel{+6}{S}$ | Fe(OH)3 |
 歼-15是中国第一代舰载战斗机,自我攻防能力突出,飞行速度快,能轻易避开敌方雷达,数秒内探测、发现并摧毁敌方海上移动目标.歼-15的机身采用的是整体钛合金大框,极大地增强了机身强度,在提高运载能力的同时也提高了飞机的使用寿命.
歼-15是中国第一代舰载战斗机,自我攻防能力突出,飞行速度快,能轻易避开敌方雷达,数秒内探测、发现并摧毁敌方海上移动目标.歼-15的机身采用的是整体钛合金大框,极大地增强了机身强度,在提高运载能力的同时也提高了飞机的使用寿命.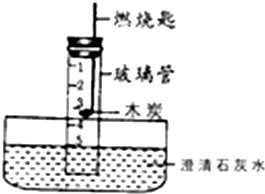 如右图进行测定空气中氧气含量实验(玻璃管分为6等分,实验前液面停留在管内5刻度处).
如右图进行测定空气中氧气含量实验(玻璃管分为6等分,实验前液面停留在管内5刻度处).