题目内容
10.20℃时,将等质量的甲、乙两种固体物质,分别加入到盛有100g水的烧杯中,充分搅拌后现象如图1,加热到50℃时现象如图2,甲、乙两种物质的溶解度曲线如图3,请结合图示回答下列问题:
(1)图1中一定为饱和溶液的是甲(选填“甲”或“乙”);
(2)图2中甲、乙两溶液中溶质质量分数的大小关系为甲=(选填“>”“<”或“=”)乙;
(3)图3中表示乙的溶解度曲线是N(选填“M”或“N”);其中P点表示的含义是30℃时,甲、乙两种固体物质的溶解度相等;
(4)在50℃下,将甲物质的不饱和溶液变为饱和溶液,可采取的方法是降温(或加溶质或蒸发溶剂).
分析 (1)根据饱和溶液的定义进行解答;
(2)根据题意可以知道图2中相同质量的溶剂溶解了相同质量的溶质,结合溶质的质量分数的计算公式可以完成解答;
(3)根据图中信息可以知道20℃时甲的溶解度小于乙的溶解度,结合图3可以完成解答,两条溶解度曲线的交点表示该点所示的温度下,两物质的溶解度是相同的,可以据此判断P点的意义
(4)根据不饱和溶液与饱和溶液的转化考虑.
解答 解:(1)从图1中可以知道甲没有完全溶解,则说明甲中形成的溶液为饱和溶液;
(2)图2中相同质量的溶剂溶解了相同质量的溶质,所以它们形成溶液的质量也相等,结合溶质的质量分数的计算公式可以知道,它们形成的溶液中溶质的质量分数也相等;
(3)根据图1中信息可以知道20℃时甲的溶解度小于乙的溶解度,而图3中在20℃时,N曲线的溶解度大于M曲线的溶解度,故N表示的是乙物质的溶解度曲线;根据溶解度曲线的意义可以知道P点表示30℃时,甲、乙两种固体物质的溶解度相等.
(4)不饱和溶液变为饱和溶液:加入溶质,蒸发溶剂或降低温度.
故答案为:(1)甲;
(2)=;
(3)N;30℃时,甲、乙两种固体物质的溶解度相等.
(4)降温(或加溶质或蒸发溶剂).
点评 解答这类题目时,首先要熟记和理解固体溶解度曲线及其使用,固体溶解度的概念和意义,溶质质量分数及其有关计算,饱和溶液和不饱和溶液的概念及其相互转变方法,以及物质的溶解和结晶的方法等相关知识;然后,根据所给的实验、问题情景或图表信息等,结合所学的相关知识和技能,最后,按照题目的要求,认真地进行选择或解答即可.

练习册系列答案
相关题目
20.为了验证Fe、Cu、Ag三种金属的金属活动性顺序,下列各组所提供的试剂无法得出结论的是( )
| A. | Fe、Ag、CuSO4溶液 | B. | Cu、FeSO4溶液、AgNO3溶液 | ||
| C. | Fe、Cu、稀盐酸、Ag | D. | Cu、Ag、FeSO4溶液 |
18.以下物质分散在水中,经搅拌过滤后,所得溶液名称正确的是( )
| A. |  氧化钙溶液 | B. |  烧碱溶液 | C. |  胆矾溶液 | D. |  食盐溶液 |
15.下列图标的实验操作正确的是( )
| A. | 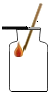 氧气验满 | B. |  取用药品 | C. | 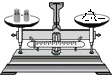 称取氯化钠 称取氯化钠 | D. | 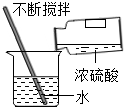 稀释浓硫酸 |
2.在购买和使用化肥时,要了解化肥的性质,以便合理施用.为了给爸爸做技术指导,小红利用自己掌握的知识对碳酸钾(K2CO3)、硫酸铵[(NH4)2SO4]两种化肥的相关性质做了以下探究.
【实验探究】
【结论与应用】碳酸钾与硫酸铵不能(填“能”或“不能”)混用,说明原因碳酸钾溶液呈碱性,与硫酸铵混合施用,产生NH3,降低肥效.
【实验探究】
| 探 究 过 程 | 实 验 现 象 | 结论及化学方程式 | |
| K2CO3 | (NH4)2SO4 | ||
| (1)配制碳酸钾、硫酸铵溶液.分别取碳酸钾和硫酸铵固体,加足量水搅拌. | 得到澄清溶液,温度无明显变化 | 得到澄清溶液,温度明显降低 | 都易溶于水,硫酸铵溶于水时吸收的热量大于放出的热量. |
| (2)猜想与假设. 碳酸钾、硫酸铵溶液的酸碱性都可能有种情况. 分别取少量两种溶液于两只试管中,滴加紫色石蕊试液. | 变蓝 | 变红 | 说明碳酸钾溶液显碱性; 说明硫酸铵溶液显 酸性. |
| (3)与盐酸反应. 分别取少量两种溶液于两只 试管中,加入稀盐酸. | 有气泡产生 | 无明显现象 | 碳酸钾能与酸反应. |
| (4)与氢氧化钠溶液反应. 分别取少量两种溶液于两只试管中,加入氢氧化钠溶液,微热. | 无明显现象 | 有气泡产生且有刺激性气味 | 硫酸铵能与碱反应.写出相关的化学方程式: (NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑ |
19.根据下列实验装置图,回答问题.
(1)写出图中仪器a的名称长颈漏斗.
(2)实验室用过氧化氢和二氧化锰制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,气体发生装置为B(填字母).
(3)实验室用石灰石和稀盐酸制取CO2的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,该反应生成的CO2中常混有少量氯化氢气体,可用盛有饱和NaHCO3溶液的F装置将其除去,混合气体应从F装置的②口(填“①”或“②”)通入.
| 发生装置 | 收集装置 | 洗气装置 |
 |  |  |
(2)实验室用过氧化氢和二氧化锰制取氧气的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,气体发生装置为B(填字母).
(3)实验室用石灰石和稀盐酸制取CO2的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,该反应生成的CO2中常混有少量氯化氢气体,可用盛有饱和NaHCO3溶液的F装置将其除去,混合气体应从F装置的②口(填“①”或“②”)通入.

 A、B、C、D、E 是初中化学中常见的物质,其中A 是天然气的主要成分,C 可用于改良酸性土壤,反应②属于分解反应.它们之间的相互转化关系如图所示:(图中“→”表示物质间存在的转化关系,部分反应条件已略去)
A、B、C、D、E 是初中化学中常见的物质,其中A 是天然气的主要成分,C 可用于改良酸性土壤,反应②属于分解反应.它们之间的相互转化关系如图所示:(图中“→”表示物质间存在的转化关系,部分反应条件已略去)