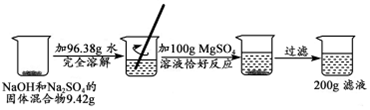
题目内容
12.地球“发烧”了材料1:空气的成分
空气是多种气体的混合物.空气的成分可分为恒定成分和易变成分两类.恒定成分是指空气中含量大,在任何地方含量几乎不变,包括78.06%氮气、20.94%氧气、0.94%氩等稀有气体,合计约占99.94%.易变成分是指在空气中含量很少,但因季节、地域等自然因素和人类的活动而引起相对含量的较大变化,甚至某些成分急剧增加或减少.如表中列出了大气中几种易变成分:
| 易变成分(浓度cm3/m3) | 变化的原因 |
| 二氧化碳 约300(约占空气的0.03%) | |
| 水蒸气约290(约占空气的0.03%) | |
| 甲烷约1.0-1.2t | 天然气泄露 |
| 氮的氧化物约0.52 | 化石燃料的燃烧 |
| 臭氧0.01-0.04 | 含氟化合物的使用 |
| 硫的化合物:二氧化硫、硫化氢等 | 化石燃料的燃烧等 |
| 一氧化碳 | 汽车尾气等 |
| 合计:0.06% |
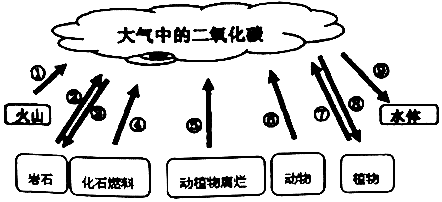
试回答下列问题:
(1)从地球上动植物生命活动所需要的物质角度看,为什么空气如此重要?
①动植物的呼吸离不开氧气;②植物的光合作用离不开二氧化碳;③生命活动离不开水,没有大气中水蒸气参与的水的天然循环,一切生命活动就不可能正常进行.
(2)大气中多余的二氧化碳从何而来?从上述材料可以看出,人类赖以生存的大气,正遭受空前严重的破坏.二氧化碳作为一种主要的温室气体,含量增加导致气候变暖、地球“发烧”、灾害频发,成为当前威胁人类生存发展最严重的问题.分析材料2,你认为导致大气中二氧化碳含量增加的直接原因是:
①化石燃料的大量使用;②森林的减少.
(3)在⑧中,消耗二氧化碳的过程叫做光合作用.在⑨中,消耗二氧化碳的反应属于化合反应(填化学反应的基本类型).在④中,以天然气(CH4)为例,燃烧反应的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
分析 从空气的成分及各成分的性质进行分析,氧气具有帮助呼吸的性质,二氧化碳参与植物的光合作用生成氧气和有机物,一切生命活动离不开水,造成空气中二氧化碳含量增加的原因主要是化石燃料的大量使用以及森林的减少,根据叙述的物质之间的反应即可写出有关反应的化学方程式.
解答 解:(1)氧气具有帮助呼吸的性质,二氧化碳参与植物的光合作用生成氧气和有机物,一切生命活动离不开水,所以本题答案为:动植物的呼吸离不开氧气,植物的光合作用离不开二氧化碳,生命活动离不开水,没有大气中水蒸气参与的水的天然循环,一切生命活动就不可能正常进行;
(2)根据材料2造成二氧化碳含量增多的原因是化石燃料的大量使用以及森林的减少;
(3)通过植物的光合作用二氧化碳能被消耗,在⑧中,消耗二氧化碳的过程叫做光合作用;在⑨中,消耗二氧化碳的反应是二氧化碳溶于水能生成碳酸,反应的化学方程式为:CO2+H2O═H2CO3,属于化合反应;
天然气的主要成分是甲烷,燃烧能生成二氧化碳和水,反应的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
答案:
(1)①动植物的呼吸离不开氧气;②植物的光合作用离不开二氧化碳;③生命活动离不开水,没有大气中水蒸气参与的水的天然循环,一切生命活动就不可能正常进行;
(2)①化石燃料的大量使用;②森林的减少;
(3)光合作用;化合;CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O
点评 本题考查了空气的重要作用以及二氧化碳含量增加的原因和有关反应方程式的书写,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
2.关于能量和能源的利用,下列说法正确的是( )
| A. | 人类大量使用太阳能会导致温室效应 | |
| B. | 因为能量是守恒的,所以不存在能源危机 | |
| C. | 现在人类社会使用的主要能源是煤、石油和天然气 | |
| D. | 核能的利用会造成放射性污染,所以应该关闭核电站 |
3.工业上常利用石灰浆[主要成分为Ca(OH)2]制备化工原料KClO3,流程如下:

已知:
①反应1为:6Cl2+6Ca(OH)2═Ca(ClO3)2+5CaCl2+6H2O.
②有关物质在常温下的溶解度如下:
(1)操作a的名称是过滤,在实验室中完成此操作需要的玻璃仪器有烧杯、玻璃棒、漏斗.
(2)反应2为复分解反应,则溶液A中含有的溶质为CaCl2和KClO3(填化学式),你认为该反应能得到KClO3晶体的原因是KClO3在常温下溶解度较小.
(3)洗涤KClO3晶体时,可选用下列BC洗涤剂(填字母编号)
A、KCl饱和溶液 B、冰水 C、饱和KClO3溶液.

已知:
①反应1为:6Cl2+6Ca(OH)2═Ca(ClO3)2+5CaCl2+6H2O.
②有关物质在常温下的溶解度如下:
| 物质 | Ca(ClO3)2 | CaCl2 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(2)反应2为复分解反应,则溶液A中含有的溶质为CaCl2和KClO3(填化学式),你认为该反应能得到KClO3晶体的原因是KClO3在常温下溶解度较小.
(3)洗涤KClO3晶体时,可选用下列BC洗涤剂(填字母编号)
A、KCl饱和溶液 B、冰水 C、饱和KClO3溶液.
20.我们常食用加碘食盐、高钙牛奶、加铁酱油等,这里的“碘”、“钙”、“铁”是指( )
| A. | 分子 | B. | 原子 | C. | 离子 | D. | 元素 |
7.氢气不同于其他气体的最显著的特性是( )
| A. | 无色 | B. | 密度最小 | C. | 难溶于水 | D. | 具有可燃性 |