题目内容
13.元素在自然界里分布并不均匀,从整个的地壳含量的多少分析,最丰富的金属元素是( )| A. | O | B. | Al | C. | Fe | D. | Si |
分析 根据地壳中各元素含量的排序及元素的分类进行分析判断.
解答 解:地壳含量较多的元素(前四种)按含量从高到低的排序为:氧、硅、铝、铁,其中含量最多的金属元素是铝元素.
故选B.
点评 本题很简单,熟记地壳里各元素的含量、了解元素的分类是正确解答本题的关键.

练习册系列答案
相关题目
4.把A、B、C、D四种物质放在密闭容器中,在一定条件下充分反应,并测得反应物和产物在反应前后各物质的质量如表所示:
下列说法正确的是( )
| 物 质 | A | B | C | D |
| 反应前质量/g | 19.7 | 8.7 | 21.6 | 0.4 |
| 反应后质量/g | 待测 | 17.4 | 0 | 3.6 |
| A. | 物质C一定是化合物,物质D可能是单质 | |
| B. | 反应后密闭容器中A的质量为19.7g | |
| C. | 反应过程中,物质B和物质D变化的质量比为87:36 | |
| D. | 若物质A与物质C的相对分子质量之比为194:216,则反应中A和C的化学计量数之比为2:1 |
1.有一包白色粉末,可能由CuSO4、Na2SO4、Na2CO3、BaCl2、NaOH中的一种或几种组成.为探究其组成,同学们查阅资料得知NaCl、BaCl2溶液呈中性,经过思考设计并进行了以下实验:

请分析实验过程,回答下列问题:
(1)白色粉末中一定不含CuSO4、Na2SO4;可能含有NaOH.
(2)生成白色沉淀的化学方程式为Na2CO3+BaCl2=BaCO3↓+2NaCl.
(3)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究.
【提出问题】无色滤液中呈碱性的物质是什么?
【作出猜想】猜想Ⅰ:Na2CO3
猜想Ⅱ:NaOH
猜想Ⅲ:Na2CO3和NaOH
【进行实验】
【得出结论】白色粉末的成分是Na2CO3、BaCl2、NaOH.

请分析实验过程,回答下列问题:
(1)白色粉末中一定不含CuSO4、Na2SO4;可能含有NaOH.
(2)生成白色沉淀的化学方程式为Na2CO3+BaCl2=BaCO3↓+2NaCl.
(3)为最终确定白色粉末的组成,还需要对无色滤液中呈碱性的物质进行探究.
【提出问题】无色滤液中呈碱性的物质是什么?
【作出猜想】猜想Ⅰ:Na2CO3
猜想Ⅱ:NaOH
猜想Ⅲ:Na2CO3和NaOH
【进行实验】
| 实验步骤 | 实验现象 | 实验结论 |
| ①取无色滤液少许于试管中,滴加BaCl2溶液 | 产生白色沉淀 | 猜想Ⅱ不成立 |
| ②在①反应后的试管中滴加无色酚酞溶液 | 溶液变为红色 | 猜想Ⅲ成立 |
8.松花蛋,又称皮蛋,皮蛋是一种中国传统美食.其中一种加工工艺的主要原料配方为:鸭蛋、水、生石灰、纯碱、食盐,加工时将纯碱、食盐加入容器中,加沸水溶解,再慢慢加入生石灰充分反应,冷却后得到料液,再加入鸭蛋浸渍.请回答下列问题:
(1)鸭蛋中富含的营养素有水和蛋白质.
(2)生石灰加入沸水中,水能持续保持沸腾,其原因是生石灰与水反应放出大量的热.
(3)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为红色.
同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】料液中除含有NaOH和NaCl外,还含有那些溶质?
【猜想】甲同学推断只有Ca(OH)2;
乙同学推断只有Na2CO3;
丙同学推断有Ca(OH)2、也有Na2CO3;
通过进一步讨论,大家一致认为丙同学的猜想是错误的,其他两个还需探究.
【实验探究】
【探究结论】甲同学的推断是正确的,请写出步骤②中发生反应的方程式:Ca(OH)2+Na2CO3═2NaOH+CaCO3↓
【问题与思考】
(1)实验①加入足量稀盐酸的目的是检验料液中是否含有碳酸钠.
(2)新做的皮蛋往往带有涩味,食用时可以加入适量的食醋.
(1)鸭蛋中富含的营养素有水和蛋白质.
(2)生石灰加入沸水中,水能持续保持沸腾,其原因是生石灰与水反应放出大量的热.
(3)静置后,取少量的上层料液,稀释后滴加无色酚酞试液,料液应变为红色.
同学们对上层料液的成分产生了兴趣,请你一起参加他们的探究活动.
【提出问题】料液中除含有NaOH和NaCl外,还含有那些溶质?
【猜想】甲同学推断只有Ca(OH)2;
乙同学推断只有Na2CO3;
丙同学推断有Ca(OH)2、也有Na2CO3;
通过进一步讨论,大家一致认为丙同学的猜想是错误的,其他两个还需探究.
【实验探究】
| 实验步骤 | 实验现象 |
| ①取少量上层料液,滴加稀盐酸 | 无明显现象 |
| ②另取少量上层料液,滴加碳酸钠溶液 | 产生白色沉淀 |
【问题与思考】
(1)实验①加入足量稀盐酸的目的是检验料液中是否含有碳酸钠.
(2)新做的皮蛋往往带有涩味,食用时可以加入适量的食醋.
5.体操运动员在完成单杠、吊环项目时常用“镁粉”搓手,以起到防滑效果.某种“镁粉”中可能含有Mg、MgO、Mg(OH)2、MgCO3中的一种或两种固体,实验小组对其成分展开了探究.
已知:MgO+2HCl=MgCl2+H2O
MgCO3+2HCl=MgCl2+H2O+CO2↑
(1)探究“镁粉”中是否含有Mg和MgCO3
(2)①取少量样品,如图1所示进行实验.观察到a试管中有气泡产生,b试管中产生的现象是澄清石灰水变浑浊,则证明“镁粉”中一定含有MgCO3.
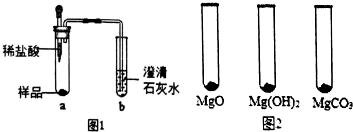
②为证明“镁粉”中是否含有Mg,小明将燃着的木条放在图中b试管口上方,木条熄灭.但同学们指出,该实验不能达成实验目的,需要将图中的澄清石灰水替换成浓NaOH溶液,目的是把二氧化碳全部吸收.小明按照修改后的实验方案重复上述实验,观察到b试管口无明显现象,证明“镁粉”中没有Mg.
(3)探究“镁粉”中是否还含有MgO及Mg(OH)2
【实验过程】
Ⅰ.用MgO、Mg(OH)2和MgCO3三种固体分别做性质实验.分别取0.5g三种固体粉末,每次取样方法如图2所示:
逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失.在下表中记录消耗的同浓度稀盐酸的体积(以下体积均在同一条件下测定,且保留到小数点后1位)
Mg(OH)2与盐酸发生中和反应的化学方程式为Mg(OH)2+2HCl=MgCl2+2H2O.
Ⅱ.取“镁粉”样品0.5g,加入上述稀盐酸至粉末恰好溶解.此时消耗稀盐酸的体积约为5.3mL.
【实验分析及结论】
“镁粉”不只含有MgCO3.理由是0.5g“镁粉”消耗稀盐酸的体积与0.5gMgCO3消耗稀盐酸的体积不相等.
【实验反思】
为确定“镁粉”的具体成分,同学们认为还需要补充如下实验:分别取0.5g“镁粉”和0.5gMgCO3,加入足量稀盐酸,测定生成的气体体积分别为119mL和140mL.由此可知“镁粉”中含有MgCO3的质量分数为85%.
已知:MgO+2HCl=MgCl2+H2O
MgCO3+2HCl=MgCl2+H2O+CO2↑
(1)探究“镁粉”中是否含有Mg和MgCO3
(2)①取少量样品,如图1所示进行实验.观察到a试管中有气泡产生,b试管中产生的现象是澄清石灰水变浑浊,则证明“镁粉”中一定含有MgCO3.

②为证明“镁粉”中是否含有Mg,小明将燃着的木条放在图中b试管口上方,木条熄灭.但同学们指出,该实验不能达成实验目的,需要将图中的澄清石灰水替换成浓NaOH溶液,目的是把二氧化碳全部吸收.小明按照修改后的实验方案重复上述实验,观察到b试管口无明显现象,证明“镁粉”中没有Mg.
(3)探究“镁粉”中是否还含有MgO及Mg(OH)2
【实验过程】
Ⅰ.用MgO、Mg(OH)2和MgCO3三种固体分别做性质实验.分别取0.5g三种固体粉末,每次取样方法如图2所示:
逐滴加入相同溶质质量分数的稀盐酸直至粉末恰好消失.在下表中记录消耗的同浓度稀盐酸的体积(以下体积均在同一条件下测定,且保留到小数点后1位)
| MgO | Mg(OH)2 | MgCO3 | |
| 消耗稀盐酸的体积/mL | 10.4 | 7.2 | 5.0 |
Ⅱ.取“镁粉”样品0.5g,加入上述稀盐酸至粉末恰好溶解.此时消耗稀盐酸的体积约为5.3mL.
【实验分析及结论】
“镁粉”不只含有MgCO3.理由是0.5g“镁粉”消耗稀盐酸的体积与0.5gMgCO3消耗稀盐酸的体积不相等.
【实验反思】
为确定“镁粉”的具体成分,同学们认为还需要补充如下实验:分别取0.5g“镁粉”和0.5gMgCO3,加入足量稀盐酸,测定生成的气体体积分别为119mL和140mL.由此可知“镁粉”中含有MgCO3的质量分数为85%.
3.今年世界水日的主题为“生命之水”.下列措施:①推广使用无磷洗衣粉;②加强工业废水的达标排放;③加快生活污水净化处理的建设;④提倡节约用水;⑤减少化肥和农药的使用量,合理的是( )
| A. | ①②③ | B. | ①②④⑤ | C. | ②③④⑤ | D. | ①②③④⑤ |
 空气中含量最多的气体是氮气;石灰水露置在空气中一段时间后,液面会形成一层白色薄膜,原因是空气中含有二氧化碳;松脆的饼干放在空气中两三天就变软了,证明了空气中含有水.如图用红磷燃烧来测定空气中氧气的含量,所发生反应的文字表达式为磷+氧气$\frac{点燃}{\;}$五氧化二磷.(本题填写出正确的化学式也给分)
空气中含量最多的气体是氮气;石灰水露置在空气中一段时间后,液面会形成一层白色薄膜,原因是空气中含有二氧化碳;松脆的饼干放在空气中两三天就变软了,证明了空气中含有水.如图用红磷燃烧来测定空气中氧气的含量,所发生反应的文字表达式为磷+氧气$\frac{点燃}{\;}$五氧化二磷.(本题填写出正确的化学式也给分)
