题目内容
9.我市某化工厂排放的尾气里含有有毒的二氧化氮(NO2),为防止其污染空气,工厂用NaOH溶液吸收二氧化氮(反应的化学方程式为:2NO2+2NaOH=NaNO3+NaNO2+H2O)
(1)NaOH中氧元素的质量分数是40%;
(2)计算:消耗NaOH溶质的质量为80kg,理论上可吸收二氧化氮的质量为多少?
分析 (1)根据物质中某元素的质量分数=$\frac{该元素相对原子质量×原子个数}{该物质相对分子质量}$×100%,进行解答.
(2)根据二氧化氮与氢氧化钠溶液反应的化学方程式和二氧化氮的质量,列出比例式,就可计算出理论上可吸收二氧化氮的质量
解答 解:(1)NaOH中氧元素的质量分数是:$\frac{16}{23+16+1}$×100%=40%;
故答案为:(1)40%.
(2)设理论上可吸收二氧化氮的质量为x,
2NO2+2NaOH=NaNO3+NaNO2+H2O
92 80
x 80kg
$\frac{92}{x}=\frac{80}{80kg}$
解得x=92kg
答:理论上可吸收二氧化氮的质量为92kg.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力,增加了学生分析问题的思维跨度,强调了学生整合知识的能力

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.在购买和使用化肥时,要了解化肥的性质,以便合理施用.为了给爸爸做技术指导,小红利用自己掌握的知识对碳酸钾(K2CO3)、硫酸铵[(NH4)2SO4]两种化肥的相关性质做了以下探究.
【实验探究】
【结论与应用】碳酸钾与硫酸铵不能(填“能”或“不能”)混用,说明原因碳酸钾溶液呈碱性,与硫酸铵混合施用,产生NH3,降低肥效.
【实验探究】
| 探 究 过 程 | 实 验 现 象 | 结论及化学方程式 | |
| K2CO3 | (NH4)2SO4 | ||
| (1)配制碳酸钾、硫酸铵溶液.分别取碳酸钾和硫酸铵固体,加足量水搅拌. | 得到澄清溶液,温度无明显变化 | 得到澄清溶液,温度明显降低 | 都易溶于水,硫酸铵溶于水时吸收的热量大于放出的热量. |
| (2)猜想与假设. 碳酸钾、硫酸铵溶液的酸碱性都可能有三种情况. 分别取少量两种溶液于两只试管中,滴加紫色石蕊试液. | 变蓝 | 变红 | 说明碳酸钾溶液显碱性; 说明硫酸铵溶液显 酸 性. |
| (3)与盐酸反应. 分别取少量两种溶液于两只试管中,加入稀盐酸. | 有气泡产生 | 无明显现象 | 碳酸钾能与酸反应. |
| (4)与氢氧化钠溶液反应. 分别取少量两种溶液于两只试管中,加入氢氧化钠溶液,微热. | 无明显现象 | 有气泡产生且有刺激性气味 | 硫酸铵能与碱反应.写出相关的化学方程式:(NH4)2SO4+2NaOH=Na2SO4+2H2O+2NH3↑ |
5.一杯20℃的硝酸钾饱和溶液,欲使其溶质的质量分数变小,下列方法可行的是( )
| A. | 加入一定量的硝酸钾 | B. | 升温到40℃ | ||
| C. | 加入一定量的水 | D. | 恒温蒸发部分水 |
4.现有镁和另一种金属组成的混合物,把2.4g该混合物加入到100g一定溶质质量分数的稀盐酸中,恰好完全反应,产生氢气的质量为a.则下列说法中正确的是( )
| A. | 若混合物为Mg、Fe,a可能是0.2g | |
| B. | 若混合物为Mg、Zn,a的值一定小于0.2g | |
| C. | 若混合物为Mg、Cu,a是0.1g,则该混合物中镁的质量分数为50% | |
| D. | 若混合物为Mg、Al,则加入的稀盐酸中溶质质量分数一定大于10% |
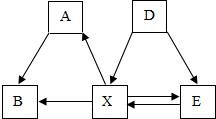 几种常见的物质之间的相互转化关系如图(各字母代表一种物质,各符号表示一个化学反应,部分反应物、生成物及反应条件略去),已知物种物质均有碳、氢、氧中的部分元素组成,A和B所含元素相同,D和E所含元素相同,X为单质,A为有毒气体,B和E可以发生化合反应.
几种常见的物质之间的相互转化关系如图(各字母代表一种物质,各符号表示一个化学反应,部分反应物、生成物及反应条件略去),已知物种物质均有碳、氢、氧中的部分元素组成,A和B所含元素相同,D和E所含元素相同,X为单质,A为有毒气体,B和E可以发生化合反应.