题目内容
17.某铁的样品5.5克(内含一种杂质),与足量的盐酸反应后,产生的氢气的质量为0.2克,则可能含有下列哪种金属( )| A. | 镁 | B. | 锌 | C. | 铝 | D. | 铜 |
分析 镁和稀盐酸反应生成氯化镁和氢气,锌和稀盐酸反应生成氯化锌和氢气,铝和稀盐酸负影视城氯化铝和氢气,铜不能和稀盐酸反应.
解答 解:镁、锌、铝、铁和稀盐酸反应的化学方程式及其金属和生成氢气的质量关系为:
Mg+2HCl═MgCl2+H2↑,Zn+2HCl═ZnCl2+H2↑,2Al+6HCl═2AlCl3+3H2↑,Fe+2HCl═FeCl2+H2↑,
24 2 65 2 54 6 56 2
由以上数据可知,当产生氢气质量是0.2g时,消耗镁、锌、铝、铁的质量分别是2.4g、6.5g、1.8g、5.6g,
铁的样品5.5g和稀盐酸反应生成的氢气质量是0.2g,说明含有的金属可能是镁,也可能是铝,不可能是锌和铜.
故选:AC.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
7.下列物质中,只有微观含义的是( )
| A. | O3 | B. | P2O5 | C. | Au | D. | 2C |
12.下列有关说法中正确的是( )
| A. | 离子都是带电的原子 | |
| B. | 不同元素最本质的区别是相对原子质量不同 | |
| C. | 在化学反应中,反应前后的原子的种类没有改变、数目没有增减 | |
| D. | 水通电产生氢气和氧气,说明水中含有氢分子和氧分子 |
17.下列装置不能达到实验目的是( )
| A. | 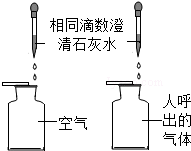 比较二氧化碳的含量 | B. |  研究二氧化锰的催化作用 | ||
| C. | 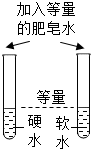 区分硬水和软水 | D. |  测定空气中氧气的含量 |
18.下列现象中,一定发生化学变化的是( )
| A. | 水结成冰 | B. | 酒精挥发 | C. | 电灯发光 | D. | 蜡烛燃烧 |
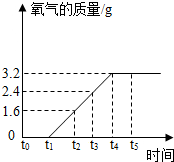 实验室制取氧气时,某同学取一定质量的高锰酸钾加热,记录产生氧气的质量与反应时间的关系如图所示,请回答下列问题:
实验室制取氧气时,某同学取一定质量的高锰酸钾加热,记录产生氧气的质量与反应时间的关系如图所示,请回答下列问题: