题目内容
15.下列图象与所对应的实验相符的是( )| A. | 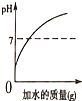 向一定质量的稀盐酸中不断加水,溶液的pH变化情况 | |
| B. | 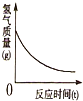 在密闭的硬质玻璃管中充满氢气,并盛有一定质量的氧化铜,加热反应时的氢气质 量变化情况 | |
| C. | 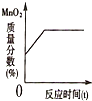 加热一定质量的氯酸钾和二氧化锰的混合物,二氧化锰在固体混合物中的质量分数 变化情况 | |
| D. | 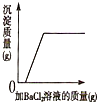 在一定质量的稀盐酸与硫酸钠的混合溶液中逐渐滴加氯化钡溶液,沉淀的变化情况 |
分析 A、根据向稀盐酸中不断加水,溶液pH的变化情况分析;
B、根据在加热时氢气与氧化铜的反应分析;
C、根据氯酸钾在加热、二氧化锰作催化剂时能分解放出氧气分析;
D、根据硫酸钠能与氯化钡反应生成了沉淀分析.
解答 解:A、向一定质量的稀盐酸中不断加水,溶液的pH逐渐变大,但不会等于7、大于7,故A错误;
B、在密闭的硬质玻璃管中充满氢气,并盛有一定质量的氧化铜,加热反应时的氢气质量逐渐变小,当完全反应时氢气的质量会等于零,故B错误;
C、加热一定质量的氯酸钾和二氧化锰的混合物,二氧化锰在固体混合物中的质量分数会逐渐变大,当氯酸钾完全分解后质量分数变为最大,故C正确;
D、在一定质量的稀盐酸与硫酸钠的混合溶液中逐渐滴加氯化钡溶液,开始就会产生沉淀,故D错误.
故选C.
点评 此题是一道反应与图象的结合题,解题的关键是能结合反应分析各种量的变化关系,利用反应与图象相结合进行分析探讨,进而作出正确的判断.

练习册系列答案
相关题目
3.关于电解水(H2O)实验的说法正确的是( )
| A. | 电解水时在正极产生氧气 | B. | 实验证明水是由氢气和氧气组成的 | ||
| C. | 水中氢、氧元素的质量比为2:1 | D. | 水分子是由氢分子和氧原子构成的 |
4.如图生活用品由有机合成材料制成的是( )
| A. |  塑料水盆 | B. |  不锈钢龙头 | C. |  木桶 | D. |  纯棉毛巾 |



 构建知识网络是一种重要的学习方法.如图是“铁”的化学性质知识网络图(“→”表示一种物质可转化为另一种物质),其中B是密度最小的气体,C为红色固体单质.请回答下列问题:
构建知识网络是一种重要的学习方法.如图是“铁”的化学性质知识网络图(“→”表示一种物质可转化为另一种物质),其中B是密度最小的气体,C为红色固体单质.请回答下列问题: 为了测定空气中氧气的含量,小华设计了如下方案:选用实际溶剂为40ml的直玻璃管作反应容器,将过量的白磷放入试管,用橡皮塞紧直玻璃管,通过导管与实际容积为60mL的且润滑性很好的针筒注射器组成如图所示的实验装置.假设此装置能按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题:
为了测定空气中氧气的含量,小华设计了如下方案:选用实际溶剂为40ml的直玻璃管作反应容器,将过量的白磷放入试管,用橡皮塞紧直玻璃管,通过导管与实际容积为60mL的且润滑性很好的针筒注射器组成如图所示的实验装置.假设此装置能按照小华的设想正常进行,且白磷所占体积与导管内的气体体积忽略不计,请回答下列问题: