题目内容
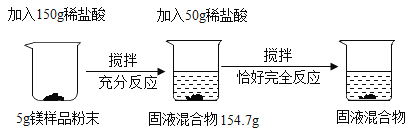
【题目】无水氯化钙的用途广泛。以石灰石矿粉(含有MgSO4、Fe2O3、SiO2等杂质)为原料,生产无水氯化钙的流程如图:

(1)过滤操作的注意事项可归纳为:“一贴二低三靠”。其中“一贴”指___________过滤后,滤液仍然浑浊的可能原因有_______________(写一种)。
(2)写出滤液1中加入BaCl2发生反应的化学方程式__________。
(3)滤渣3中的固体除有Ca(OH)2外,还有_____________(写化学式)。
(4)对滤液3调节pH值时发生反应的化学方程式为_______________。
【答案】滤纸紧贴漏斗的内壁 承接滤液的烧杯不干净或倾倒液体时液面高于滤纸边缘或滤纸破损 ![]() Mg(OH)2、Fe(OH)3
Mg(OH)2、Fe(OH)3 ![]()
【解析】
(1)过滤的操作要领可归纳为“一贴、两低、三靠”,“一贴”指滤纸紧贴漏斗的内壁,否则会使过滤的速率变慢;滤纸破损或液面高于滤纸边缘(浊液从滤纸与漏斗缝隙流下,起不到过滤作用)或仪器不干净都可能导致滤液仍旧浑浊;
(2)石灰石矿粉含有CaCO3、MgSO4、Fe2O3、SiO2等物质,加入过量稀盐酸,CaCO3与盐酸反应生成氯化钙、二氧化碳和水,Fe2O3与盐酸反应生成氯化铁和水,MgSO4与盐酸不反应,能溶于水,故过滤后滤渣为SiO2,滤液1中有MgSO4、CaCl2、FeCl3、HCl,向滤液中加入适量氯化钡溶液,与其中的硫酸镁反应生成硫酸钡沉淀和氯化镁,方程式为:![]() ;
;
(3)向滤液1(MgSO4、CaCl2、FeCl3、HCl)中加入适量![]() ,MgSO4与之恰好完全反应,过滤,滤渣2为
,MgSO4与之恰好完全反应,过滤,滤渣2为![]() ,滤液2为CaCl2、FeCl3、HCl、
,滤液2为CaCl2、FeCl3、HCl、![]() ;向滤液2中加入石灰乳
;向滤液2中加入石灰乳![]() ,会与FeCl3、HCl、
,会与FeCl3、HCl、![]() 发生反应,题目中问滤渣3除了石灰乳还有谁,表明石灰乳是过量的,故FeCl3、HCl、
发生反应,题目中问滤渣3除了石灰乳还有谁,表明石灰乳是过量的,故FeCl3、HCl、![]() 都被反应完,方程式分别为
都被反应完,方程式分别为![]() 、
、![]() 、
、![]() ;故滤渣3中除了Ca(OH)2外,还有Mg(OH)2、Fe(OH)3;
;故滤渣3中除了Ca(OH)2外,还有Mg(OH)2、Fe(OH)3;
(4)由石灰乳过量,故滤液3中有除有CaCl2,还有![]() ;对滤液3调节pH值时,需要加入酸中和掉多余的
;对滤液3调节pH值时,需要加入酸中和掉多余的![]() ,为保证最后得到产品氯化钙,应选择加入稀盐酸,反应的化学方程式为:
,为保证最后得到产品氯化钙,应选择加入稀盐酸,反应的化学方程式为:![]() 。
。

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
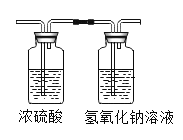
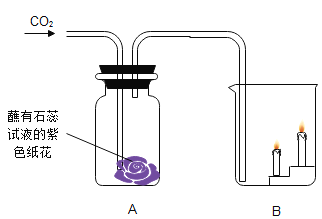
英语小英雄天天默写系列答案【题目】小刚将制得的二氧化碳气体依次通过下图所示的装置,在A、B两装置中他可观察到的实验现象和得出的结论。
| A装置 | B装置 |
现象________ | 现象_________ | |
该变化的化学方程式为_________ | 验证的性质________ |