题目内容
12.15℃时,食盐的溶解度是 35g,求此时食盐饱和溶液的溶质的质量分数.分析 根据饱和溶液中溶质质量分数=$\frac{溶解度}{溶解度+100g}×$100%,进行分析解答.
解答 解:15℃时,食盐的溶解度是 35g,此时食盐饱和溶液的溶质的质量分数为$\frac{35g}{35g+100g}$×100%≈25.9%.
答:此时食盐饱和溶液的溶质的质量分为25.9%.
点评 本题难度不大,掌握饱和溶液中溶质质量分数=$\frac{溶解度}{溶解度+100g}×$100%是正确解答本题的关键.

练习册系列答案
相关题目
2.下列实验操作正确的是( )
| A. | 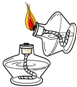 点燃酒精灯 | B. | 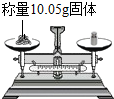 | C. | 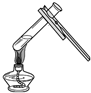 液体加热 | D. | 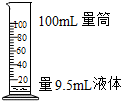 |
3.同学们用高锰酸钾制氧气.制取结束清洗仪器.发现加热高锰酸钾的试管内壁有用水洗刷不掉的黑色固体.
问题一:黑色固体是什么?
【交流讨论1】同学们结合实验现象和对高锰酸钾及其分解产物的了解.进行分析判断.
【实验验证1】向未洗净的试管中加入某种液体,产生能使带火星木条复燃的气体.证明上述判断正确.加入的液体是过氧化氢溶液.
问题二:用什么洗掉MnO2?
【交流讨论2】MnO2与Na2CO3、Ba(OH)2、Fe2O3、Zn中的某一种物质组成最相近,理由是二氧化锰和氧化铁都属于氧化物.这种物质能与稀盐酸反应,化学方程式为Fe2O3+6HCl═2FeCl3+3H2O,由此推测MnO2也能与稀盐酸反应.
【实验验证2】向未洗净的试管中加入稀盐酸,黑色固体没有变化.
【交流讨论3】实验说明同一类物质的化学性质不一定相同.MnO2有什么化学性质,用什么试剂清洗呢?同学们请教老师后决定用草酸(H2C2O4)溶液试一试.
【实验验证3】向未洗净的试管中加入草酸溶液,黑色固体果然被除去,同时发现产生许多气泡.
问题三:产生了什么气体?
【交流讨论4】根据质量守恒定律,所以产生的气体可能为CO2、CO、H2、O2等.
【实验验证4】将该气体通入澄清石灰水中,发现澄清石灰水变浑浊,证明该气体是CO2.
问题一:黑色固体是什么?
【交流讨论1】同学们结合实验现象和对高锰酸钾及其分解产物的了解.进行分析判断.
| 判断 | 依据 |
| 不是KMnO4 | KMnO4能溶于水形成紫红色溶液 |
| 不是K2MnO4(填化学式) | 冲洗试管时出现深绿色溶液,说明该物质能溶于水 |
| 是MnO2 | 它是不溶于水的黑色固体 |
问题二:用什么洗掉MnO2?
【交流讨论2】MnO2与Na2CO3、Ba(OH)2、Fe2O3、Zn中的某一种物质组成最相近,理由是二氧化锰和氧化铁都属于氧化物.这种物质能与稀盐酸反应,化学方程式为Fe2O3+6HCl═2FeCl3+3H2O,由此推测MnO2也能与稀盐酸反应.
【实验验证2】向未洗净的试管中加入稀盐酸,黑色固体没有变化.
【交流讨论3】实验说明同一类物质的化学性质不一定相同.MnO2有什么化学性质,用什么试剂清洗呢?同学们请教老师后决定用草酸(H2C2O4)溶液试一试.
【实验验证3】向未洗净的试管中加入草酸溶液,黑色固体果然被除去,同时发现产生许多气泡.
问题三:产生了什么气体?
【交流讨论4】根据质量守恒定律,所以产生的气体可能为CO2、CO、H2、O2等.
【实验验证4】将该气体通入澄清石灰水中,发现澄清石灰水变浑浊,证明该气体是CO2.
20.推理是一种重要的学习方法,下列推理正确的是( )
| A. | 化学变化都遵循质量守恒定律,所以质量不发生改变的变化就是化学变化 | |
| B. | 化合物是由多种元素组成的纯净物,所以由多种元素组成的纯净物一定是化合物 | |
| C. | 最外层达8电子的微粒化学性质稳定,因此化学性质稳定的微粒最外层电子数都是8 | |
| D. | 燃烧是发光、放热的变化,所以有发光、放热现象的变化一定是燃烧 |
7.实验室制取二氧化碳,结合下列实验装置回答有关问题:

Ⅰ.实验室制取二氧化碳气体常用的药品是稀盐酸、大理石(填名称),该反应的化学方程式是CaCO3+2HCl=CaCl2+CO2↑+H2O;若将产生的二氧化碳导入澄清石灰水中,会观察到的现象是澄清石灰水变浑浊,发生反应的方程式是Ca(OH)2+C02=CaCO3↓+H20.
Ⅱ.如图中能控制反应发生和停止的装置是C(填字母).
②制取二氧化碳后剩余溶液的成分探究(假设二氧化碳已完全放出, 杂质不溶于水且不参加反应):
杂质不溶于水且不参加反应):
Ⅰ.甲、乙同学分析认为剩余溶液中一定有氯化钙,可能有盐酸.为验证是否含有盐酸,他们采用了不同方法进行实验,得到了相同的结论.
查找资料:氯化钙溶液呈中性
Ⅱ.请写出乙同学实验过程中发生反应的化学方程式Na2CO3+2HCl=2NaCl+CO2↑+H2O.

Ⅰ.实验室制取二氧化碳气体常用的药品是稀盐酸、大理石(填名称),该反应的化学方程式是CaCO3+2HCl=CaCl2+CO2↑+H2O;若将产生的二氧化碳导入澄清石灰水中,会观察到的现象是澄清石灰水变浑浊,发生反应的方程式是Ca(OH)2+C02=CaCO3↓+H20.
Ⅱ.如图中能控制反应发生和停止的装置是C(填字母).
②制取二氧化碳后剩余溶液的成分探究(假设二氧化碳已完全放出,
 杂质不溶于水且不参加反应):
杂质不溶于水且不参加反应):Ⅰ.甲、乙同学分析认为剩余溶液中一定有氯化钙,可能有盐酸.为验证是否含有盐酸,他们采用了不同方法进行实验,得到了相同的结论.
查找资料:氯化钙溶液呈中性
| 实验操作 | 实验现象 | 结论 | |
| 甲 | 取样于试管中,滴加紫色石蕊试液 | 试液变红 | 有盐酸 |
| 乙 | 取样于试管中,逐滴滴加碳酸钠溶液至过量 | 有气泡冒出 |
17.如图基本实验操作正确的是( )
| A. |  检查气密性 | B. |  测量溶液的pH | C. |  取固体药品 | D. |  熄灭酒精灯 |
 构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题:
构建模型和构建知识网络是化学学习中重要的学习方法,李华同学利用左手构建酸的性质知识网络,如图所示,请结合图示回答下列问题: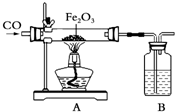 钢铁的冶炼是人类文明的一个重要标志,如图是模拟炼铁的实验装置图.
钢铁的冶炼是人类文明的一个重要标志,如图是模拟炼铁的实验装置图.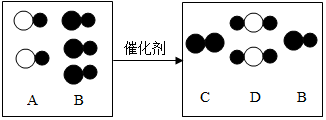
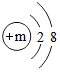 ,其微粒符号可表示为X2,则m的值为8.
,其微粒符号可表示为X2,则m的值为8.