题目内容
18.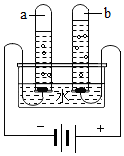 通过电解水的方法得到氧气.
通过电解水的方法得到氧气. (l)检验b试管内气体的方法是将带火星的木条伸入试管,带火星的木条复燃,证明该气体是氧气.
(2)此探究实验的目的是探究水的组成.
分析 (1)根据电解水生成气体的性质分析回答;
(2)根据实验的过程分析实验的目的.
解答 解:(l)由电解水的实验装置可知,b试管内的气体是电源的正极产生的气体是氧气,具有助燃性,检验方法是:将带火星的木条伸入试管,带火星的木条复燃,证明该气体是氧气.
(2)此探究实验生成了氢气和氧气,证明了水是由氢、氧元素组成的,所以实验的目的是:探究水的组成.
故答为:(1)将带火星的木条伸入试管,带火星的木条复燃,证明该气体是氧气;(2)探究水的组成.
点评 本题的难度不大,了解电解水的试验现象、结论、目的等即可分析解答.

练习册系列答案
相关题目
17.把少量的下列物质分别放入水中,充分搅拌,可以得到溶液的是( )
| A. | 食盐 | B. | 面粉 | C. | 泥土 | D. | 汽油 |
3.某学校化学兴趣小组的同学想测定某同学家装修后剩余大理石中碳酸钙的含量,做了如下实验:首先称取50g该大理石样品,然后将200g的稀盐酸分5次加入(假设其中的杂质既不溶于水也不与盐酸反应)进行充分反应.实验过程中的数据记录如下:
(1)a的数值为30
(2)写出实验中发生反应的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O
(3)根据已知条件列出求解生成二氧化碳总质量(x)的比例式$\frac{100}{45g}=\frac{44}{x}$
(4)大理石中碳酸钙的含量为90%.
| 稀盐酸的质量 | 第一次40g | 第二次40g | 第三次40g | 第四次40g | 第五次40g |
| 剩余固体质量 | 40g | a | 20g | l0g | 5g |
(2)写出实验中发生反应的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O
(3)根据已知条件列出求解生成二氧化碳总质量(x)的比例式$\frac{100}{45g}=\frac{44}{x}$
(4)大理石中碳酸钙的含量为90%.
10.如图所示的变化中,属于化学变化的是( )
| A. |  蒸发食盐水 | B. |  干冰升化 | C. |  面粉爆炸 | D. |  石油的分馏 |
 请你对小林、小伟两同学的实验探究方案的合理性进行反思:
请你对小林、小伟两同学的实验探究方案的合理性进行反思: 如图是一种打火机的示意图.
如图是一种打火机的示意图. 