题目内容
10.下列有关实验现象的描述正确的是( )| A. | 向氢氧化钠溶液中逐滴加入硫酸铜溶液,出现蓝色絮状沉淀 | |
| B. | 硫在氧气中燃烧,发出淡蓝色火焰,产生二氧化硫气体 | |
| C. | 铁丝在空气中燃烧,火星四射,生成黑色固体 | |
| D. | 白磷在空气中剧烈燃烧,产生大量白雾 |
分析 A、根据向氢氧化钠溶液中逐滴加入硫酸铜溶液的现象进行分析判断.
B、根据硫在氧气中燃烧燃烧的现象进行分析判断.
C、根据铁丝在空气中不能燃烧进行分析判断.
D、根据白磷在空气中燃烧的现象进行分析判断.
解答 解:A、向氢氧化钠溶液中逐滴加入硫酸铜溶液,会生成蓝色沉淀氢氧化铜,所以溶液中会出现蓝色絮状沉淀,故选项说法正确.
B、硫在空气中燃烧燃烧,产生二氧化硫气体是实验结论,不是现象,故选项说法错误.
C、铁丝在空气中不能燃烧,氧气的 浓度不够,故选项说法错误.
D、红磷在空气中燃烧,产生大量的白烟,而不是白雾,故选项说法错误.
故选:A.
点评 本题难度不大,掌握常见物质燃烧的现象即可正确解答,在描述物质燃烧的现象时,需要注意烟和雾、实验结论和实验现象的区别.

练习册系列答案
 期末1卷素质教育评估卷系列答案
期末1卷素质教育评估卷系列答案
相关题目
20.下列防止金属锈蚀的措施中,不正确的是( )
| A. | 雨淋后的自行车及时擦干并涂上石蜡油 | |
| B. | 铁制品放在干燥的环境中 | |
| C. | 铁制品表面的铁锈用作防护层 | |
| D. | 金属容器的表面涂上一层油漆 |
1.环境问题已成为制约社会发展和进步的严重问题.有下列几种说法:
①臭氧层的主要作用是吸收紫外线;
②温室效应将导致全球气候变暖;
③酸雨主要是由于空气受到硫的氧化物和氮的氧化物污染所致;
④光化学烟雾主要由汽车排放的尾气引起的.
其中正确的是( )
①臭氧层的主要作用是吸收紫外线;
②温室效应将导致全球气候变暖;
③酸雨主要是由于空气受到硫的氧化物和氮的氧化物污染所致;
④光化学烟雾主要由汽车排放的尾气引起的.
其中正确的是( )
| A. | 只有①和② | B. | 只有②和③ | C. | 只有①、②和③ | D. | ①②③④全都正确 |
18.在学校的科技活动周上,同学们做实验时发现,将镁条放入CuSO4溶液中,镁条表面有气泡产生,对于这一异常现象产生的原因,同学们设计了以下方案进行探究.其中没有意义的是( )
| A. | 甲同学用镁粉与CuSO4 溶液反应,观察产生气泡的快慢 | |
| B. | 乙同学推测该气体可能是氢气,并收集气体用点燃法检验 | |
| C. | 丙同学猜想CuSO4 溶液呈酸性,并用pH 试纸检验 | |
| D. | 丁同学用锌粉与CuSO4 溶液反应,观察是否有气泡产生 |
5.一氧化氮是无色气体,难溶于水,密度比空气略大,在空气中能与氧气迅速反应生成红棕色的二氧化氮.在实验中,收集一氧化氮时可选用的收集方法是( )
| A. | 向上排空气法 | B. | 向下排空气法 | ||
| C. | 排水集气法或向下排空气法 | D. | 排水集气法 |
15.元素的化学性质,主要决定于( )
| A. | 核内质子数 | B. | 最外层电子数 | C. | 中子数 | D. | 原子核外电子数 |
19.某化学兴趣小组在实验室发现了一瓶标签受到腐蚀(如图所示)的无色溶液,他们对此产生了兴趣.
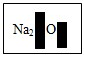
【提出问题】这瓶溶液究竟是什么?
经过询问实验老师得知,这瓶物色溶液应该是碳酸钠、碳酸氢钠、氧化钠、硫酸钠、硝酸钠中的一种.为了确定该药品,他们首先根据标签上残留的信息进行如下分析:
(1)小明认为组成中含有氧元素,该溶液一定不是NaCl氯化钠溶液.
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是这二者的化学式中Na元素的右下角不会是2.
为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验:
【设计实验】
【实验结论】
(3)这瓶无色溶液是Na2CO3.生成白色沉淀过程的化学方程式是BaCl2+Na2CO3═BaCO3↓+2NaCl.
【实验反思】
(4)小强认为上述设计实验还可简化,仍能达到目的.小强的实验操作是取少量无色溶液样品于试管中,慢慢滴加稀盐酸,看是否产生气泡少量无色溶液样品于试管中,慢慢滴加稀盐酸,看是否产生气泡.经查阅资料得知上述五种盐里碳酸钠、碳酸氢钠的溶液呈碱性,其余三种盐的溶液呈中性,请你再设计一种实验方法,确定该溶液究竟是哪种盐.简述实验操作和现象在玻璃片上放一小片pH试纸,将样品液滴到试纸上,把试纸显示的颜色与标准比色卡比较,测得溶液pH大于7.(或取少量无色溶液样品于试管中,滴加几滴无色酚酞,观察到溶液变红等.).

【提出问题】这瓶溶液究竟是什么?
经过询问实验老师得知,这瓶物色溶液应该是碳酸钠、碳酸氢钠、氧化钠、硫酸钠、硝酸钠中的一种.为了确定该药品,他们首先根据标签上残留的信息进行如下分析:
(1)小明认为组成中含有氧元素,该溶液一定不是NaCl氯化钠溶液.
(2)小英提出,碳酸氢钠、硝酸钠也不可能,你认为她的依据是这二者的化学式中Na元素的右下角不会是2.
为了确定该溶液究竟是剩余两种盐的哪一种,他们设计了如下实验:
【设计实验】
| 实验操作 | 实验现象 |
| 取少量样品于试管中,慢慢滴加BaCl2溶液,静置一段时间,倾去上层清液,向沉淀中继续滴加稀盐酸 | 先出现白色沉淀,后产生大量气泡 |
(3)这瓶无色溶液是Na2CO3.生成白色沉淀过程的化学方程式是BaCl2+Na2CO3═BaCO3↓+2NaCl.
【实验反思】
(4)小强认为上述设计实验还可简化,仍能达到目的.小强的实验操作是取少量无色溶液样品于试管中,慢慢滴加稀盐酸,看是否产生气泡少量无色溶液样品于试管中,慢慢滴加稀盐酸,看是否产生气泡.经查阅资料得知上述五种盐里碳酸钠、碳酸氢钠的溶液呈碱性,其余三种盐的溶液呈中性,请你再设计一种实验方法,确定该溶液究竟是哪种盐.简述实验操作和现象在玻璃片上放一小片pH试纸,将样品液滴到试纸上,把试纸显示的颜色与标准比色卡比较,测得溶液pH大于7.(或取少量无色溶液样品于试管中,滴加几滴无色酚酞,观察到溶液变红等.).
20.有关实验现象的描述正确的是( )
| A. | 硫在空气中燃烧发出明亮的蓝紫色火焰 | |
| B. | 铁丝在氧气中剧烈燃烧,火星四射 | |
| C. | 干冰在空气中升华,周围出现白色烟雾 | |
| D. | 碳在空气中剧烈燃烧,发出白光 |
