题目内容
12.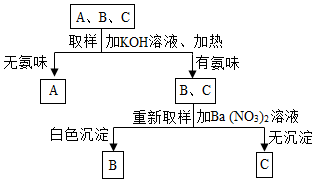 鉴别(NH4 )2 SO4、NH4 NO3、NaNO3 三种无色溶液,随机编号为A、B、C,实验过程及现象如图所示:
鉴别(NH4 )2 SO4、NH4 NO3、NaNO3 三种无色溶液,随机编号为A、B、C,实验过程及现象如图所示:(1)A 中的溶质是NaNO3;
(2)B 与 Ba(NO 3 )2 溶液混合:
①反应的化学方程式为(NH4 )2 SO4+Ba(NO 3 )2=BaSO4↓+2NH4NO3;
②过滤,分别列出滤液中所含溶质 的所有可能情况.只有硝酸铵、硝酸铵和硫酸铵的混合物、硝酸铵和硝酸钡的混合物.
分析 根据铵态氮肥和碱混合加热会生成有刺激性气味的氨气,硫酸根离子和钡离子反应会生成硫酸钡沉淀等知识进行分析.
解答 解:铵态氮肥和碱混合加热会生成有刺激性气味的氨气,硫酸根离子和钡离子反应会生成硫酸钡沉淀,
(1)A、B、C三种无色溶液加入氢氧化钠溶液、加热,A中没有氨味,B、C有氨味,所以A是硝酸钠溶液;
(2)重取样品,加入硝酸钡,B中会生成白色沉淀,所以B是硫酸铵,硫酸铵和硝酸钡反应生成硫酸钡沉淀和硝酸铵,化学方程式为:(NH4 )2 SO4+Ba(NO 3 )2=BaSO4↓+2NH4NO3;
硫酸铵和硝酸钡可能恰好完全反应,可能其中的一种物质过量,所以过滤,分别列出滤液中所含溶质的所有可能情况是:只有硝酸铵、硝酸铵和硫酸铵的混合物、硝酸铵和硝酸钡的混合物.
故答案为:(1)NaNO3;
(2):(NH4 )2 SO4+Ba(NO 3 )2=BaSO4↓+2NH4NO3;
只有硝酸铵、硝酸铵和硫酸铵的混合物、硝酸铵和硝酸钡的混合物.
点评 在解此类题时,首先分析被鉴别物质的性质,然后选择适当的试剂和方法,出现不同的现象即可鉴别.

练习册系列答案
相关题目
5.下列实验设计,不能达到实验目的是( )


| A. | ①证明CO2密度比空气大且不支持燃烧 | |
| B. | ②验证质量守恒定律 | |
| C. | ③说明不同的物体着火点不同 | |
| D. | ④测定空气中氧气的含量 |
1.有关下列结构示意图的说法正确的是( )


| A. | 第1组的原子在化学反应中都易失去电子 | |
| B. | 第3、4组的原子都可以形成由离子构成的化合物 | |
| C. | 第2组的粒子化学性质相似 | |
| D. | 第1组的原子位于元素周期表中的同一周期 |
2.下列关于金属的说法错误的是( )
| A. | 铝制品抗腐蚀能力较铁制品强 | |
| B. | 不能再铁制容器配制波尔多液 | |
| C. | 铁和稀硫酸反应的化学方程式为:2Fe+3H2SO4═Fe2(SO4)3+3H2↑ | |
| D. | 用CuSO4溶液、Fe和Ag三种物质可以验证Fe、Cu、Ag三种金属的活动性强弱顺序 |





