题目内容
4.在夏天养鱼师傅向鱼塘中撒一种主要成分是过氧化钙(CaO2)的微黄色的固体.小燕同学回家后查阅资料,知道CaO2与水反应的原理是:2CaO2+2H2O=2Ca(OH)2+O2↑.(1)若需要制取3.2千克的氧气,需要CaO2多少千克?
(2)请你说出氢氧化钙在水产养殖中的作用.
分析 根据氧气的质量和对应的化学方程式求算过氧化钙的质量.氢氧化钙本身又名消石灰,可以对水体消毒.
解答 解:设需要的过氧化钙的质量为x
2CaO2+2H2O=2Ca(OH)2+O2↑
144 32
x 3.2kg
$\frac{144}{32}$=$\frac{x}{3.2kg}$
x=14.4kg
氢氧化钙本身又名消石灰,可以对水体消毒
答:(1)若需要制取3.2千克的氧气,需要CaO214.4千克?
(2)氢氧化钙在水产养殖中的作用为消毒.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
17.化学就在我们身边,化学与生活息息相关.
(1)下表为某食品包装袋的部分说明:
请回答下列问题:
①在饼干的配料中,富含蛋白质的是鸡蛋.
②碳酸氢钠的俗称小苏打;在医疗上,它是治疗胃酸过多症的一种药剂.
③考虑到营养均衡,把榨好的蔬菜汁放在面粉中和面,做成口味独特、营养丰富的蔬菜馒头,这种馒头提供的主要营养素是糖类和维生素.
(2)交警通过酒精检测仪显示的颜色变化,可快速检测出司机是否酒后驾车,其反应原理为2CrO3(红色)+3C2H5OH+3H2SO4=Cr2(SO4)3(绿色)+3CH3CHO+6X,X的化学式为H2O.
(1)下表为某食品包装袋的部分说明:
| 商品名称 | ××饼干 |
| 配料 | 小麦粉、白砂糖、精炼植物油、鸡蛋、食盐、食品添加剂(碳酸氢铵、碳酸氢钠、柠檬酸等) |
| 规格 | 180g |
| 保质期 | 10个月 |
①在饼干的配料中,富含蛋白质的是鸡蛋.
②碳酸氢钠的俗称小苏打;在医疗上,它是治疗胃酸过多症的一种药剂.
③考虑到营养均衡,把榨好的蔬菜汁放在面粉中和面,做成口味独特、营养丰富的蔬菜馒头,这种馒头提供的主要营养素是糖类和维生素.
(2)交警通过酒精检测仪显示的颜色变化,可快速检测出司机是否酒后驾车,其反应原理为2CrO3(红色)+3C2H5OH+3H2SO4=Cr2(SO4)3(绿色)+3CH3CHO+6X,X的化学式为H2O.
19.对某pH=2的溶液中溶质成分进行分析、检测,下列结果合理的是( )
| A. | KNO3 K2CO3 CaCl2 | B. | KC1 NaHCO3 K2SO4 | ||
| C. | NaCl ZnSO4 KOH | D. | HC1 MgCl2 Na2SO4 |
9.为了探究影响物质溶解性的因素,设计了如表所示的实验方案.该实验 无法探究的因素是( )
| 实验序号 | 溶质 | 溶剂 | 温度 |
| 1 | 蔗糖 | 水 | 20℃ |
| 2 | 蔗糖 | 水 | 40℃ |
| 3 | 食盐 | 水 | 40℃ |
| 4 | 食盐 | 植物油 | 40℃ |
| A. | 溶质种类 | B. | 溶剂种类 | C. | 溶液温度 | D. | 颗粒粗细 |
16.如表是KCl固体在不同温度时的溶解度.下列说法错误的是( )
| 温度/℃ | 0 | 20 | 40 | 60 | 80 |
| 溶解度/g | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 |
| A. | KCl固体的溶解度随温度的升高而增大 | |
| B. | 60℃的KCl饱和溶液降温后会有晶体析出 | |
| C. | 80℃时,KCl固体的溶解度是51.1g | |
| D. | 20℃时,KCl饱和溶液的溶质质量分数为34.0% |
13.下列实验基本操作中正确的是( )
| A. | 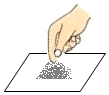 | B. | 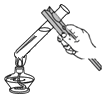 | C. | 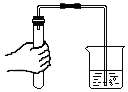 | D. | 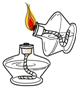 |
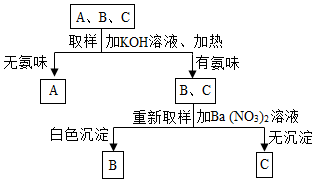 鉴别(NH4 )2 SO4、NH4 NO3、NaNO3 三种无色溶液,随机编号为A、B、C,实验过程及现象如图所示:
鉴别(NH4 )2 SO4、NH4 NO3、NaNO3 三种无色溶液,随机编号为A、B、C,实验过程及现象如图所示: 水是一种重要的资源. 如图是活性炭净水器示意图,其中活性炭的作用是:吸附色素和异味、滤去不溶性杂质.用此装置得到了澄清透明的水,该水是否为纯水,理由不是纯水,净化后的水中含有可燃性的杂质.
水是一种重要的资源. 如图是活性炭净水器示意图,其中活性炭的作用是:吸附色素和异味、滤去不溶性杂质.用此装置得到了澄清透明的水,该水是否为纯水,理由不是纯水,净化后的水中含有可燃性的杂质.