题目内容
下列说法中,错误的是( )
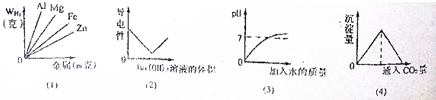

| A、等质量的Al、Mg、Fe、Zn四种金属分别与足量盐酸反应产生的H2质量与消耗的金属质量关系如图(1) |
| B、表示向稀硫酸中滴加Ba(OH)2溶液时,溶液的导电性与Ba(OH)2溶液的体积的变化关系如图(2) |
| C、表示向一定量的H2SO4溶液中加水时,溶液的pH与所加水的质量的变化关系如图(3) |
| D、将CO2连续通入澄清石灰水,生成沉淀的量(纵坐标)与通入CO2量(横坐标)的关系如图(4) |
考点:金属的化学性质,二氧化碳的化学性质,碱的化学性质,酸碱溶液的稀释
专题:元素化合物知识型
分析:A、在金属质量相同时,化合价也相同的条件下,相对分子质量越小的产生的氢气的质量越多,若化合价不同,则利用计算公式=
计算生成氢气的质量.
B、硫酸与氢氧化钡反应生成硫酸钡和水,随着氢氧化钡的加入,溶液中离子的浓度逐渐降低,导电性降低,当硫酸与氢氧化钡恰好反应时,溶液中的离子浓度几乎为零,导电性几乎为零,继续滴加氢氧化钡溶液,溶液导电性又增强.
C、硫酸显酸性,pH小于7,水的pH等于7,向一定量的H2SO4溶液中加水时,溶液的pH逐渐升高,但不会超过7.
D、澄清的石灰水中通入二氧化碳,先产生白色沉淀,后沉淀又消失.
| 化合价 |
| 相对分子质量 |
B、硫酸与氢氧化钡反应生成硫酸钡和水,随着氢氧化钡的加入,溶液中离子的浓度逐渐降低,导电性降低,当硫酸与氢氧化钡恰好反应时,溶液中的离子浓度几乎为零,导电性几乎为零,继续滴加氢氧化钡溶液,溶液导电性又增强.
C、硫酸显酸性,pH小于7,水的pH等于7,向一定量的H2SO4溶液中加水时,溶液的pH逐渐升高,但不会超过7.
D、澄清的石灰水中通入二氧化碳,先产生白色沉淀,后沉淀又消失.
解答:解:A、在金属质量相同时,化合价也相同的条件下,相对分子质量越小的产生的氢气的质量越多,若化合价不同,则利用计算公式=
计算生成氢气的质量,所以各种金属和酸反应产生氢气的质量是:镁
=0.083,铝
=0.11,铁
=0.036,锌
=0.03,所以产生氢气质量的由多到少的顺序是Al、Mg、Fe、Zn,故图象正确.
B、硫酸与氢氧化钡反应生成硫酸钡和水,随着氢氧化钡的加入,溶液中离子的浓度逐渐降低,导电性降低,当硫酸与氢氧化钡恰好反应时,溶液中的离子浓度几乎为零,导电性几乎为零,继续滴加氢氧化钡溶液,溶液导电性又增强,故图象正确;
C、硫酸显酸性,pH小于7,水的pH等于7,向一定量的H2SO4溶液中加水时,溶液的pH逐渐升高,但不会超过7,故图象错误;
D、石灰水中先通入二氧化碳,先发生Ca(OH)2+CO2═CaCO3↓+H2O,因此生成沉淀,后发生CaCO3+CO2+H2O=Ca(HCO3)2,沉淀消失,且生成沉淀和溶解沉淀消耗的二氧化碳的质量比是1:1,故图象正确.
故选C.
| 化合价 |
| 相对分子质量 |
| 2 |
| 24 |
| ,3 |
| 27 |
| 2 |
| 56 |
| 2 |
| 65 |
B、硫酸与氢氧化钡反应生成硫酸钡和水,随着氢氧化钡的加入,溶液中离子的浓度逐渐降低,导电性降低,当硫酸与氢氧化钡恰好反应时,溶液中的离子浓度几乎为零,导电性几乎为零,继续滴加氢氧化钡溶液,溶液导电性又增强,故图象正确;
C、硫酸显酸性,pH小于7,水的pH等于7,向一定量的H2SO4溶液中加水时,溶液的pH逐渐升高,但不会超过7,故图象错误;
D、石灰水中先通入二氧化碳,先发生Ca(OH)2+CO2═CaCO3↓+H2O,因此生成沉淀,后发生CaCO3+CO2+H2O=Ca(HCO3)2,沉淀消失,且生成沉淀和溶解沉淀消耗的二氧化碳的质量比是1:1,故图象正确.
故选C.
点评:此题难度不大,明确发生的化学反应及反应与图象的对应关系是解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
如图是元素周期表中第三周期元素的原子结构示意图:
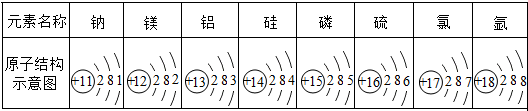
依据如图判断,下列结论正确的是( )

依据如图判断,下列结论正确的是( )
| A、12 号元素的原子,在化学反应中容易得到电子变成离子 |
| B、钠元素与硫元素形成化合物的化学式为Na2S |
| C、第三周期元素的化学性质相似 |
| D、Cl→Cl-,则 Cl 核内有 18 个质子 |
下列变化不属于缓慢氧化的是( )
| A、铁生锈 | B、人类呼吸 |
| C、木炭燃烧 | D、食物腐烂 |
下列实验操作叙述正确的是( )
| A、倾倒液体时,试剂瓶口颈挨着试管口快速倒入 |
| B、制取气体时,先装药品,后检查装置的气密性 |
| C、胶头滴管应垂直悬空在试管口上方,向试管中滴加液体 |
| D、称量任何固体药品时,均要在天平的左右托盘上各放一张相同的纸片 |