题目内容
我校九年级化学兴趣小组选用下图所示装置,进行有关气体的制取和性质实验,请你共同参与探究,来回答下列问题:
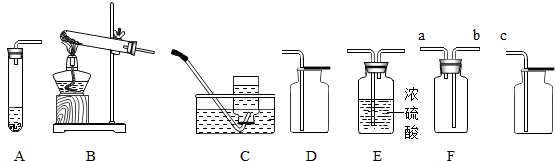
(1)写出有标号仪器的名称:a ,b .
(2)实验室用高锰酸钾制取并收集到干燥的氧气,应选用的发生装置和收集装置的配套组合为 (填装置序号).实验时要在试管口放一团棉花,其作用是 ;若再用排水法收集氧气的合适时机是 .
(3)实验室制取二氧化碳时选用的药品为 和 ,发生反应时的化学方程式为 ,请分析不能用稀硫酸替代其中液体药品的原因是 .收集CO2时只能用D装置是因为 .
(4)若F装置中盛有紫色的石蕊溶液,通入CO2气体后,石蕊溶液将变色的情形为 ,其中起变色作用的物质是 ,则用化学方程式表示 .若F装置中盛有 ,则可用于检验二氧化碳.

(1)写出有标号仪器的名称:a
(2)实验室用高锰酸钾制取并收集到干燥的氧气,应选用的发生装置和收集装置的配套组合为
(3)实验室制取二氧化碳时选用的药品为
(4)若F装置中盛有紫色的石蕊溶液,通入CO2气体后,石蕊溶液将变色的情形为
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,二氧化碳的实验室制法,二氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)依据常见化学仪器的名称完成;
(2)依据常用气体的发生装置和收集装置及有关注意事项分析作答;
(3)依据实验室制取二氧化碳的原理及注意事项分析作答;
(4)依据二氧化碳的化学性质分析作答.
(2)依据常用气体的发生装置和收集装置及有关注意事项分析作答;
(3)依据实验室制取二氧化碳的原理及注意事项分析作答;
(4)依据二氧化碳的化学性质分析作答.
解答:解:
(1)有标号仪器的名称:a是导气管,b也是导气管;
(2)实验室用高锰酸钾制取并收集到干燥的氧气,应选用的发生装置为B、而后利用装置E进行干燥、再利用D装置收集气体;故应选用的发生装置和收集装置的配套组合为:BED;为防止加热时高锰酸钾被导出导气管,实验时要在试管口放一团棉花;用排水法收集氧气的合适时机是有气泡从水槽中导气管口连续均匀冒出;
(3)实验室制取二氧化碳时选用的药品为碳酸钙和盐酸;反应时的化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O;稀硫酸与碳酸钙反应生成的硫酸钙会沉积覆盖在碳酸钙表面,使反应发生缓慢甚至停止,所以不能用稀硫酸替代盐酸;
(4)二氧化碳能溶于水,且密度比空气大,.收集CO2时只能用D装置.
故答案为:
(1)导气管;导气管;
(2)BED;防止加热时高锰酸钾被导出导气管;有气泡从水槽中导气管口连续均匀冒出;
(3)碳酸钙;盐酸;CaCO3+2HCl═CaCl2+CO2↑+H2O;稀硫酸与碳酸钙反应生成的硫酸钙会沉积覆盖在碳酸钙表面,使反应发生缓慢甚至停止;二氧化碳能溶于水,且密度比空气大;
(4)由紫色变为变为红色;碳酸;CO2+H2O═H2CO3;澄清石灰水.
(1)有标号仪器的名称:a是导气管,b也是导气管;
(2)实验室用高锰酸钾制取并收集到干燥的氧气,应选用的发生装置为B、而后利用装置E进行干燥、再利用D装置收集气体;故应选用的发生装置和收集装置的配套组合为:BED;为防止加热时高锰酸钾被导出导气管,实验时要在试管口放一团棉花;用排水法收集氧气的合适时机是有气泡从水槽中导气管口连续均匀冒出;
(3)实验室制取二氧化碳时选用的药品为碳酸钙和盐酸;反应时的化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O;稀硫酸与碳酸钙反应生成的硫酸钙会沉积覆盖在碳酸钙表面,使反应发生缓慢甚至停止,所以不能用稀硫酸替代盐酸;
(4)二氧化碳能溶于水,且密度比空气大,.收集CO2时只能用D装置.
故答案为:
(1)导气管;导气管;
(2)BED;防止加热时高锰酸钾被导出导气管;有气泡从水槽中导气管口连续均匀冒出;
(3)碳酸钙;盐酸;CaCO3+2HCl═CaCl2+CO2↑+H2O;稀硫酸与碳酸钙反应生成的硫酸钙会沉积覆盖在碳酸钙表面,使反应发生缓慢甚至停止;二氧化碳能溶于水,且密度比空气大;
(4)由紫色变为变为红色;碳酸;CO2+H2O═H2CO3;澄清石灰水.
点评:本题主要考查了氧气和二氧化碳的反应装置、反应原理、操作步骤和注意事项,掌握相关知识即可正确解答.

练习册系列答案
相关题目
下列仪器不宜用于做化学反应容器的有( )
| A、试管 | B、烧杯 | C、量筒 | D、燃烧匙 |
小芳阅读课外书籍得知,SO2+Ca (OH)2=CaSO3↓ (白色)+H2O,SO2+H2O=H2SO3(弱酸)从而获得以下结论,其中错误的是( )
| A、能使澄清石灰水变浑浊的气体不一定是二氧化碳 |
| B、能使紫色石蕊溶液变红的气体不一定是二氧化碳 |
| C、可用排水集气法收集二氧化硫 |
| D、可用闻气味法鉴别二氧化碳和二氧化硫 |
 某校兴趣小组同学准备进行常见酸、碱的性质实验时,发现有一装无色溶液的试剂瓶未盖瓶盖且标签破损(如图1),于是决定对这瓶溶液进行实验探究:
某校兴趣小组同学准备进行常见酸、碱的性质实验时,发现有一装无色溶液的试剂瓶未盖瓶盖且标签破损(如图1),于是决定对这瓶溶液进行实验探究: