题目内容
根据要求写出下列方程式,并在括号内注明基本反应类型.
(1)铜丝插入硝酸银溶液中: ;
(2)正常雨水呈弱酸性的原因: ;
(3)含有硫酸的废水用熟石灰来处理 反应.
(1)铜丝插入硝酸银溶液中:
(2)正常雨水呈弱酸性的原因:
(3)含有硫酸的废水用熟石灰来处理
考点:书写化学方程式、文字表达式、电离方程式,反应类型的判定
专题:化学用语和质量守恒定律
分析:(1)铜的金属活动性比银的强,故铜能把硝酸银的溶液中的银置换出来,发生的反应为置换反应;
(2)根据二氧化碳会与雨水反应生成碳酸进行分析,
(3)由题意,可知反应物为氢氧化铝和稀盐酸,生产物为氯化铝和水,则可书写化学方程式;
(2)根据二氧化碳会与雨水反应生成碳酸进行分析,
(3)由题意,可知反应物为氢氧化铝和稀盐酸,生产物为氯化铝和水,则可书写化学方程式;
解答:解:
(1)铜丝放入硝酸银的溶液中,发生的反应为置换反应,故反应式为:Cu+2AgNO3=2Ag+Cu(NO3)2;反应属于置换反应;
(2))二氧化碳和水反应生成碳酸,碳酸具有弱酸性,反应式为:CO2+H2O=H2CO3;反应属于化合反应;
(3)由题意,可知反应物和生产物,则可书写化学方程式为:Ca(OH)2+H2SO4═CaSO4↓+2H2O;反应符合AB+CD=AD+CB的特点,故属于复分解反应;
故答案为:
(1)Cu+2AgNO3=2Ag+Cu(NO3)2;置换反应;
(2)CO2+H2O=H2CO3;化合反应;
(3)Ca(OH)2+H2SO4═CaSO4↓+2H2O;复分解;
(1)铜丝放入硝酸银的溶液中,发生的反应为置换反应,故反应式为:Cu+2AgNO3=2Ag+Cu(NO3)2;反应属于置换反应;
(2))二氧化碳和水反应生成碳酸,碳酸具有弱酸性,反应式为:CO2+H2O=H2CO3;反应属于化合反应;
(3)由题意,可知反应物和生产物,则可书写化学方程式为:Ca(OH)2+H2SO4═CaSO4↓+2H2O;反应符合AB+CD=AD+CB的特点,故属于复分解反应;
故答案为:
(1)Cu+2AgNO3=2Ag+Cu(NO3)2;置换反应;
(2)CO2+H2O=H2CO3;化合反应;
(3)Ca(OH)2+H2SO4═CaSO4↓+2H2O;复分解;
点评:确定反应物、生成物、反应条件,正确书写化学方程式;并且掌握书写化学方程式的方法和步骤.

练习册系列答案
相关题目
下列溶液无色,在pH=1时能大量共存的是( )
| A、K2SO4 AgNO3 NaCl |
| B、Na2SO4 NH4Cl ZnCl2 |
| C、Na2SO4 KCl NaNO3 |
| D、CuSO4 NaCl KNO3 |
中考来临之际,妈妈为小宇设计了一份午餐食谱:米饭、麻辣豆腐、红烧排骨,从“合理膳食”的角度分析,这份午餐还需要增加的食物是( )
| A、炒青菜 | B、小米粥 |
| C、鸡蛋羹 | D、牛奶 |
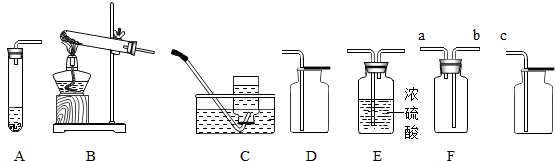
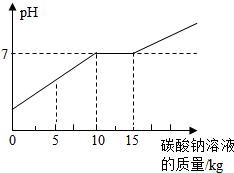 某班同学做完“二氧化碳的制取和性质”的分组实验后,将废液缸里上层清液都倒入一个废液桶中,化学兴趣小组做了如下实验:
某班同学做完“二氧化碳的制取和性质”的分组实验后,将废液缸里上层清液都倒入一个废液桶中,化学兴趣小组做了如下实验: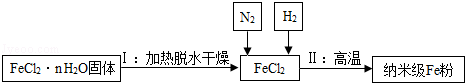
 某次实验中,关闭?装置的弹簧夹,通过长颈漏斗向试管中加水,发现水充满了整个试管,该现象说明
某次实验中,关闭?装置的弹簧夹,通过长颈漏斗向试管中加水,发现水充满了整个试管,该现象说明