题目内容
6.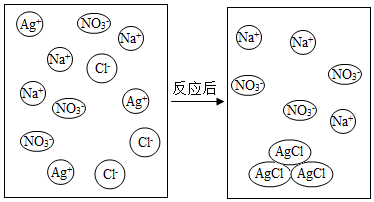 如图是氯化钠溶液和硝酸银溶液反应的示意图.
如图是氯化钠溶液和硝酸银溶液反应的示意图.(1)溶液中还存在的一种微粒是H2O(用化学符号表示);
(2)该反应的本质是银离子和氯离子结合生成沉淀;
(3)写出与上述反应本质相同的另一化学方程式(反应物之一仍为AgNO3):HCl+AgNO3═AgCl↓+HNO3.
分析 (1)根据溶液的组成分析;
(2)由反应的微观过程示意图,从构成从微观粒子的角度分析该反应酸与碱中和的实质;
(3)硝酸银与可溶性的氯化物反应实质都为银离子和氯根离子生成氯化银沉淀.
解答 解:(1)溶液由溶质和溶剂组成,所以溶液中还存在水,所以还存在的一种微粒是H2O,
(2)由反应的微观过程示意图,该反应的实质是银离子和氯离子生成氯化银沉淀.
(3)硝酸银与可溶性的氯化物反应实质都为银离子和氯根离子生成氯化银沉淀,所以盐酸与硝酸银反应属于这一原理,化学方程式为:HCl+AgNO3═AgCl↓+HNO3.
故答案为:(1)H2O(2)银离子;氯离子(3)HCl+AgNO3═AgCl↓+HNO3.
点评 本题难度不大,掌握常见化学符号的书写方法、学会从微观的角度看物质是正确解答此类题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.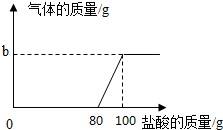 在实验室中,化学兴趣小组的同学发现了一瓶敞口的氢氧化钠固体.他们对该固体的成分进行了定量实验分析:称取固体21.3克放入锥形瓶中,加入一定量的水配制成50克溶液,再向锥形瓶中依次滴加20克盐酸充分反应.测得部分数据与图象如表.请根据有关信息回答问题.
在实验室中,化学兴趣小组的同学发现了一瓶敞口的氢氧化钠固体.他们对该固体的成分进行了定量实验分析:称取固体21.3克放入锥形瓶中,加入一定量的水配制成50克溶液,再向锥形瓶中依次滴加20克盐酸充分反应.测得部分数据与图象如表.请根据有关信息回答问题.
(1)a的数值为110,b的数值为2.2.
(2)兴趣小组的同学通过实验,得出该试剂已部分变质的结论,其依据是(通过实验数据和图象做出你的分析)滴加盐酸至80g时,开始时有二氧化碳生成,证明有碳酸钠存在,之前滴加的盐酸无现象,说明了盐酸与氢氧化钠反应,从而证明氢氧化钠存在.
(3)计算该固体中氢氧化钠的质量(写出具体的计算过程).
 在实验室中,化学兴趣小组的同学发现了一瓶敞口的氢氧化钠固体.他们对该固体的成分进行了定量实验分析:称取固体21.3克放入锥形瓶中,加入一定量的水配制成50克溶液,再向锥形瓶中依次滴加20克盐酸充分反应.测得部分数据与图象如表.请根据有关信息回答问题.
在实验室中,化学兴趣小组的同学发现了一瓶敞口的氢氧化钠固体.他们对该固体的成分进行了定量实验分析:称取固体21.3克放入锥形瓶中,加入一定量的水配制成50克溶液,再向锥形瓶中依次滴加20克盐酸充分反应.测得部分数据与图象如表.请根据有关信息回答问题. | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 | 第6次 | |
| 加入盐酸的质量 | 20 | 20 | 20 | 20 | 20 | 20 |
| 锥形瓶中物质的质量 | 70 | 90 | a | 130 | 147.8 | 167.8 |
(2)兴趣小组的同学通过实验,得出该试剂已部分变质的结论,其依据是(通过实验数据和图象做出你的分析)滴加盐酸至80g时,开始时有二氧化碳生成,证明有碳酸钠存在,之前滴加的盐酸无现象,说明了盐酸与氢氧化钠反应,从而证明氢氧化钠存在.
(3)计算该固体中氢氧化钠的质量(写出具体的计算过程).
17.下列物质中氮元素的化合价最高的是( )
| A. | NH3 | B. | N2 | C. | HNO3 | D. | NO2 |
14.下列说法中不正确的是( )
| A. | 自然界中的元素是有限的,但组成的物质却是无限的 | |
| B. | 宏观上相对静止的物体,其构成微粒也是静止的 | |
| C. | 物质都具有两面性,既可以造福人类,也可能造成危害 | |
| D. | 化学变化是有规律可循的,如化学变化往往伴随着能量的变化 |
11.下列性质属于物质的化学性质的是( )
| A. | 硬度 | B. | 溶解性 | C. | 稳定性 | D. | 挥发性 |
18.下列化肥与熟石灰混合研磨后,能闻到氨气气味的是( )
| A. | 硫酸铵 | B. | 尿素 | C. | 氯化钠 | D. | 硝酸钾 |
15.下列实验设计不能达到目的是( )
| A. | 用盐酸验证敞口放置的NaOH溶液已变质 | |
| B. | 用闻气味的方法区别醋酸和食盐水溶液 | |
| C. | 石灰石高温受热分解,可用于制备生石灰 | |
| D. | 用燃烧木条的方法制备纯净的二氧化碳气体 |