题目内容
金属材料包括纯金属和合金,在工农业生产和科学研究中有广泛的应用.
(1)从金属活动性顺序表里找出三种金属X、Y、Z,它们的活动性满足X>Y>Z,能够发生如下化学反应:
①X+YSO4═XSO4+Y
②Y+2ZNO3═2Z+Y(NO3)2
③X+H2SO4═XSO4+H2↑
④Z+H2SO4不发生反应
符合要求的X、Y、Z可能分别是什么纯金属?
(2)下面是工业冶炼生铁的实验室模拟装置.在硬质玻璃管中放入药品后,先通入一氧化碳的原因是什么?结合实验现象说明如何判断反应中生成了什么物质?

(1)从金属活动性顺序表里找出三种金属X、Y、Z,它们的活动性满足X>Y>Z,能够发生如下化学反应:
①X+YSO4═XSO4+Y
②Y+2ZNO3═2Z+Y(NO3)2
③X+H2SO4═XSO4+H2↑
④Z+H2SO4不发生反应
符合要求的X、Y、Z可能分别是什么纯金属?
(2)下面是工业冶炼生铁的实验室模拟装置.在硬质玻璃管中放入药品后,先通入一氧化碳的原因是什么?结合实验现象说明如何判断反应中生成了什么物质?

考点:金属活动性顺序及其应用,铁的冶炼
专题:金属与金属材料
分析:(1)在金属活动性顺序中,氢前的金属能置换出酸中的氢,位置越靠前,反应的越剧烈,位置在前的金属能把位于其后的金属从其盐溶液中置换出来;然后根据①②③④中的反应情况推测各金属之间的活动性,再结合化合价分析.
(2)根据一氧化碳的可燃性及实验现象分析.
(2)根据一氧化碳的可燃性及实验现象分析.
解答:解:(1)解:由①可以得出,X>Y,排除选项B和C,由②可以得出,Y>Z,由③可知X>H,由④可知H>Z故三种金属的活泼性X>Y>Z.又因为XSO4可知X显+2价,可能为镁、铁或锌;又因为ZNO3可知Z显+1价,可能为银;又因为YSO4可知Y显+2价,且X>Y,可能为铁或锌;所以符合要求的X、Y、Z可能分别是镁、铁、银或镁、锌、银或锌、铁、银.
(2)一氧化碳具有可燃性,点燃不纯的一氧化碳可能发生爆炸,因此实验前要先通入一氧化碳,排净装置内的空气,防止加热时发生爆炸,加热时红色的氧化铁粉末变成黑色,说明生成了铁粉;生成的二氧化碳使澄清石灰水变浑浊;
故答案为:(1)镁、铁、银或镁、锌、银或锌、铁、银(2)先通入一氧化碳,排净装置内的空气,防止加热时发生爆炸;
加热时红色的氧化铁粉末变成黑色,说明生成了铁粉;澄清石灰水变浑浊,生成的二氧化碳.
(2)一氧化碳具有可燃性,点燃不纯的一氧化碳可能发生爆炸,因此实验前要先通入一氧化碳,排净装置内的空气,防止加热时发生爆炸,加热时红色的氧化铁粉末变成黑色,说明生成了铁粉;生成的二氧化碳使澄清石灰水变浑浊;
故答案为:(1)镁、铁、银或镁、锌、银或锌、铁、银(2)先通入一氧化碳,排净装置内的空气,防止加热时发生爆炸;
加热时红色的氧化铁粉末变成黑色,说明生成了铁粉;澄清石灰水变浑浊,生成的二氧化碳.
点评:本题考查了金属活动性顺序的应用、一氧化碳还原氧化铁的原理、实验现象及操作注意事项,完成此题,可以依据金属活动性顺序的意义以及金属活动性顺序进行.

练习册系列答案
相关题目
下列化学方程式正确的是( )
A、Mg+O2
| ||||
B、H2O
| ||||
C、4Fe+3O2
| ||||
D、2KMnO4
|
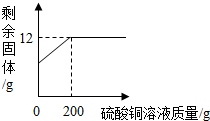 某兴趣小组想探究某生铁中铁的质量分数,现取两份质量和组成一样的生铁样品,一份与稀盐酸混合,一份与硫酸铜溶液混合,杂质不溶于水,也不参加化学反应,得到相关数据如表(图):
某兴趣小组想探究某生铁中铁的质量分数,现取两份质量和组成一样的生铁样品,一份与稀盐酸混合,一份与硫酸铜溶液混合,杂质不溶于水,也不参加化学反应,得到相关数据如表(图):