题目内容
12.根据下列粒子结构示意图,回答问题.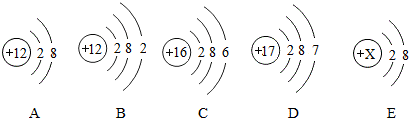
(1)E粒子带1个单位正电荷,则X=11.
(2)如图A、B、C、D四种粒子共表示三种元素,元素的种类决定于质子数.
(3)D原子在化学反应中易得到(填“得到”或“失去”)电子,元素的化学性质决定于最外层电子数.
(4)由B元素和D元素组成的化合物的化学式为MgCl2.
(5)上述结构示意图中具有相对稳定结构的是AE.
分析 (1)带1个单位正电荷说明失去了一个电子;(2)决定元素种类的是质子数;(3)最外层电子数大于4,易得电子;(4)根据化学式的书写方法考虑;(5)最外层电子数是8,属于稳定结构.
解答 解:(1)带1个单位正电荷说明失去了一个电子,所以X=2+8+1=11;
(2)决定元素种类的是质子数,所以A、B、C、D四种粒子共表示三种元素;元素的种类决定于质子数;
(3)最外层电子数大于4,易得电子,所以D原子在化学反应中易得电子,元素的化学性质决定于原子最外层电子数;
(4)B是镁,易失去2个电子,显+2价,氯元素最外层7个电子,易得一个电子显-1价,所以化学式是:MgCl2;
(5)最外层电子数是8,属于稳定结构所以上述结构示意图中具有相对稳定结构的是AE.
故答案为:(1)11;(2)三;质子数;(3)得到;最外层电子数;(4)MgCl2;AE.
点评 解答本题关键是熟悉原子结构示意图,知道决定元素种类的是质子数.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目