题目内容
6.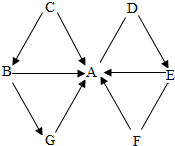 图中A~G均是初中化学常见物质,它们之间的转化或相互反应关系均为初中常见反应,其中G属于单质,且被称为最理想能源,其余均为化合物,B和C物质类别相同,D、E溶于水所得溶液的pH大于7.图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去.
图中A~G均是初中化学常见物质,它们之间的转化或相互反应关系均为初中常见反应,其中G属于单质,且被称为最理想能源,其余均为化合物,B和C物质类别相同,D、E溶于水所得溶液的pH大于7.图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去.(1)写出物质D的俗名生石灰,E的化学式Ca(OH)2;
(2)满足图中关系的物质F,可能属于下列类别中①③④(填序号)
①酸 ②碱 ③盐 ④氧化物 ⑤单质
(3)写出化学方程式:
B→G:Mg+2HCl═MgCl2+H2↑;E→A:Ca(OH)2+CO2═CaCO3↓+H2O.
分析 根据A~G均是初中化学常见物质,G属于单质,且被称为最理想能源,其余均为化合物,所以G是氢气,氢气会转化成A,所以A是水,B会转化成氢气和水,所以B是酸,B和C物质类别相同,所以C也是酸,C会转化成B,所以C是硫酸,B是盐酸,硫酸和氯化钡反应生成硫酸钡沉淀和盐酸,硫酸和碱反应生成水,D、E溶于水所得溶液的pH大于7,D会与水反应,所以D是氧化钙,D会生成E,所以E是氢氧化钙,F会转化成水,会与氢氧化钙反应,所以F是酸、盐、氧化物,然后将推出的物质进行验证即可.
解答 解:(1)A~G均是初中化学常见物质,G属于单质,且被称为最理想能源,其余均为化合物,所以G是氢气,氢气会转化成A,所以A是水,B会转化成氢气和水,所以B是酸,B和C物质类别相同,所以C也是酸,C会转化成B,所以C是硫酸,B是盐酸,硫酸和氯化钡反应生成硫酸钡沉淀和盐酸,硫酸和碱反应生成水,D、E溶于水所得溶液的pH大于7,D会与水反应,所以D是氧化钙,D会生成E,所以E是氢氧化钙,F会转化成水,会与氢氧化钙反应,所以F是酸、盐、氧化物,经过验证,推导正确,所以D是氧化钙,俗称生石灰,E的化学式是Ca(OH)2;
(2)通过推导可知,满足图中关系的物质F有酸、氧化物、盐,故选:①③④;
(3)B→G的反应是镁和盐酸反应生成氯化镁和氢气,化学方程式为:Mg+2HCl═MgCl2+H2↑,E→A的反应是氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,化学方程式为:Ca(OH)2+CO2═CaCO3↓+H2O.
故答案为:(1)生石灰,Ca(OH)2;
(2)①③④;
(3)Mg+2HCl═MgCl2+H2↑,Ca(OH)2+CO2═CaCO3↓+H2O.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 2012年4月央视曝光,不法企业为谋取暴利,用工业明胶生产“毒胶囊”,造成有的药用空心胶囊铬超标,倍受社会各界关注.铬在元素周期表中的部分信息如图,下列说法中正确的是( )
2012年4月央视曝光,不法企业为谋取暴利,用工业明胶生产“毒胶囊”,造成有的药用空心胶囊铬超标,倍受社会各界关注.铬在元素周期表中的部分信息如图,下列说法中正确的是( )| A. | 铬元素属于非金属元素 | B. | 铬元素的相对原子质量为52.00克 | ||
| C. | 铬元素原子的核电荷数为24 | D. | 该元素在地壳中的含量为52.00% |
| A. |  | B. |  | C. |  | D. |  |
| 选项 | 实验目的 | 方案1 | 方案2 |
| A | 鉴别氯化钾固体和碳酸氢铵固体 | 加水溶解 | 加熟石灰研磨 |
| B | 区分黄铜(铜锌合金)和黄金 | 加稀盐酸 | 在空气中加热 |
| C | 鉴别羊毛织品与涤纶织品 | 观察颜色 | 点燃闻气味 |
| D | 清洗铁制品表面的铁锈 | 加稀盐酸 | 用水洗涤 |
| A. | A | B. | B | C. | C | D. | D |
 我国铟的生产规模居世界同类企业首位.图1是元素周期表中铟元素的信息,图2是铟原子的结构示意图,下列说法不正确的是( )
我国铟的生产规模居世界同类企业首位.图1是元素周期表中铟元素的信息,图2是铟原子的结构示意图,下列说法不正确的是( )| A. | 图2表示的微粒属于铟元素 | B. | 该元素的相对原子质量为114.8 | ||
| C. | 该元素是金属元素 | D. | 图2表示的微粒的化学符号是In3+ |
| A. | 过氧比苯甲酰由三种元素组成 | |
| B. | 过氧化苯甲酰中碳和氧元素质量比为21:8 | |
| C. | 过氧化苯甲酰中含有14个碳原子、10个氢原子和4个氧原子 | |
| D. | 过氧化苯甲酰中碳元素的质量分数为69.4% |
(一)用图1进行实验,请回答:

(1)写出装置图中标号仪器的名称①试管,②集气瓶.
(2)写出实验室用A装置加热混有二氧化锰的氯酸钾固体制取氧气的化学方程式2KClO3 $\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
(3)写出实验室用B装置制取二氧化碳的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
(二)兴趣小组用图2所示装置探究炼铁的原理,请回答有关问题:

(1)实验进行一段时间之后,A玻璃管内观察到的现象是红色粉末变黑.
(2)利用C和D装置收集CO,CO应该从d导管口通入C装置.(填“b”或“d”)
(三)已知废铁屑的主要成份是铁,同时还有少量铁锈(Fe2O3),动物饲料硫酸亚铁的生产工艺之一如下图所示:(提示:Fe2(SO4)3+Fe═3FeSO4)

(1)反应器所在的厂房要严禁烟火、加强通风的原因是排出具有可燃性的氢气,以防爆炸;
(2)滤液M中的溶质是FeSO4、H2SO4(填化学式);
(3)在实验室中完成操作A的玻璃仪器有:玻璃棒、烧杯和漏斗;
(4)滤液M经过操作B可得硫酸亚铁晶体(FeSO4•7H2O).已知硫酸亚铁的溶解度和析出晶体的组成如表:
| 温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
 如图是硝酸钾和氯化钠的溶解度曲线.
如图是硝酸钾和氯化钠的溶解度曲线.