题目内容
15.在一定量的盐酸中加入氢氧化钠溶液.分析反应过程,回答问题.(1)氢氧化钠与稀盐酸反应的化学方程式为NaOH+HCl=NaCl+H2O;
(2)若向混合后的溶液中滴入两滴酚酞溶液,溶液呈无色,此时NaOH一定完全反应,溶液中一定含有溶质是NaCl.
分析 (1)根据氢氧化钠与稀盐酸反应生成氯化钠和水解答;
(2)根据已有的知识进行分析,氢氧化钠的水溶液呈碱性,能使酚酞溶液变红,盐酸呈酸性不能使酚酞溶液变红,氢氧化钠能与盐酸反应生成氯化钠和水,氯化钠的水溶液呈中性,不能使酚酞溶液变红解答.
解答 解:
(1)氢氧化钠与稀盐酸反应生成氯化钠和水,反应的化学方程式为:NaOH+HCl=NaCl+H2O;
(2)若向混合后的溶液中滴入两滴酚酞溶液,溶液呈无色,说明溶液呈酸性或中性,此时NaOH一定完全反应,盐酸可能有剩余,无法确定,故溶液中一定含有溶质是氯化钠.
答案:
(1)NaOH+HCl=NaCl+H2O
(2)NaOH NaCl
点评 本题考查了酸碱中和反应,完成此题,可以依据已有的知识进行,要求同学们熟记常见酸碱溶液的酸碱性与pH的关系,以便灵活应用.

练习册系列答案
 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
4.下列纺织材料中.属于合成纤维的是( )
| A. | 棉花 | B. | 腈纶 | C. | 羊毛 | D. | 蚕丝 |
5.下列有关能源的叙述正确的是( )
| A. | 石油是一种可再生资源 | |
| B. | 大量使用化石能源会造成大气污染,因此应该停止化石能源的开采和利用 | |
| C. | 人类需要的能量都是由化学反应产生的 | |
| D. | 目前没有大量使用氢能源,是由于氢气的制取成本高,贮存困难 |
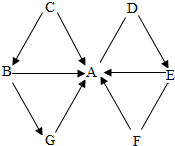 图中A~G均是初中化学常见物质,它们之间的转化或相互反应关系均为初中常见反应,其中G属于单质,且被称为最理想能源,其余均为化合物,B和C物质类别相同,D、E溶于水所得溶液的pH大于7.图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去.
图中A~G均是初中化学常见物质,它们之间的转化或相互反应关系均为初中常见反应,其中G属于单质,且被称为最理想能源,其余均为化合物,B和C物质类别相同,D、E溶于水所得溶液的pH大于7.图中“-”表示两端的物质能发生化学反应,“→”表示物质间存在转化关系,反应条件、部分反应物和生成物已略去.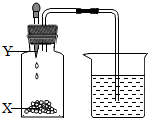 如图所示,瓶中X为固体,当把滴管内的液体Y滴入瓶中时,伸入烧杯中的导气管内上升一段水柱的是( )
如图所示,瓶中X为固体,当把滴管内的液体Y滴入瓶中时,伸入烧杯中的导气管内上升一段水柱的是( ) 哈尔滨的特产“大列巴”面包和酒糖全国闻名,吃过的人都赞不绝口.
哈尔滨的特产“大列巴”面包和酒糖全国闻名,吃过的人都赞不绝口.