题目内容
5.如图Na2CO3溶液和CaCl2溶液发生反应的“示意图”.请判断下列说法中错误的是( )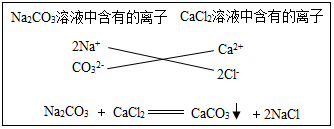
| A. | 该反应属于复分解反应 | B. | 反应前后溶液的pH值降低 | ||
| C. | 反应前后,溶液总质量保持不变 | D. | 反应能进行,是因为有沉淀生成 |
分析 Na2CO3溶液和CaCl2溶液生成碳酸钙沉淀和氯化钠,据此结合Na2CO3溶液和CaCl2溶液发生反应的“示意图”,进行分析解答.
解答 解:A、Na2CO3溶液和CaCl2溶液生成碳酸钙沉淀和氯化钠,该反应是两种化合物相互交换成分生成两种新的化合物的反应,属于复分解反应,故选项说法正确.
B、Na2CO3溶液和CaCl2溶液生成碳酸钙沉淀和氯化钠,Na2CO3溶液显碱性,生成的氯化钠溶液显中性,随着反应的进行,碱性逐渐减弱,溶液的pH值降低,故选项说法正确.
C、Na2CO3溶液和CaCl2溶液生成碳酸钙沉淀和氯化钠,由于有沉淀生成,由质量守恒定律,反应后溶液总质量减少,故选项说法错误.
D、由复分解反应发生的条件,反应能进行,是因为有沉淀生成,故选项说法正确.
故选:C.
点评 本题难度不大,掌握盐的化学性质、复分解反应的实质(离子之间结合成沉淀、气体或水)是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.熟石灰是一种常见的化学药品,下列关于熟石灰的说法错误的是( )
| A. | 熟石灰可以用作建筑材料是因为它与空气中的二氧化碳气体反应生成了不溶于水的碳酸钙 | |
| B. | 杭州富阳制造宣纸常用熟石灰制浆,这是因为熟石灰具有腐蚀性 | |
| C. | 冬季往往定期向道路两旁的树干上刷上石灰水,是因为氢氧离子有一定的杀菌作用 | |
| D. | 熟石灰可以用来检验二氧化碳等酸性气体 |
1.观察如图所呈现的实验现象,可以得出的结论是( )
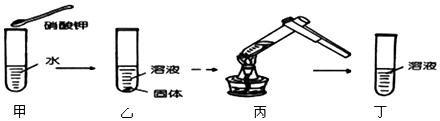

| A. | 乙图中溶液一定是饱和溶液 | |
| B. | 乙图中溶液一定是浓溶液 | |
| C. | 丁图中溶液一定是饱和溶液 | |
| D. | 丁图中溶液的溶质质量分数一定比乙图中溶液溶质质量分数小 |
13.化学反应伴随着能量的变化.下列过程中的能量变化不是由化学反应引起的是( )
| A. | 天然气燃烧 | |
| B. | 过氧化氢溶液用二氧化锰为催化剂制取氧气的反应 | |
| C. | 冰的融化 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体反应 |
20.下列现象中,属于化学变化的是( )
| A. | 樟脑丸放在衣橱中逐渐消失 | B. | 木材做成课桌 | ||
| C. | 食物腐败 | D. | 石蜡熔化 |
10.以下实验思路合理的是( )
| A. | 用酚酞试液可区分食盐溶液和盐酸溶液 | |
| B. | 常温下可用Fe与AgCl反应制取Ag | |
| C. | 可用过量的Cu(OH)2除去CuSO4溶液中少量的H2SO4 | |
| D. | 向某固体中加入稀盐酸有气泡产生,可证明该物质中一定含有CO32- |
17.下列现象中发生化学变化的是( )
| A. | 石蜡熔化 | B. | 纸张燃烧 | C. | 玻璃破碎 | D. | 酒精挥发 |
15.某同学在实验室进行有关浓硫酸的实验,观察到瓶上的标签如下表所示.他从瓶中倒出100毫升用于配制稀硫酸.求:
(1)这100毫升浓硫酸的质量是多少克?其中含溶质硫酸多少克?
(2)若将这100毫升浓硫酸与500克水均匀混合,所得稀硫酸的质量分数是多少?
| 浓硫酸500毫升 | |
| 溶质的质量分数 | 98% |
| 密度 | 1.84克/厘米3 |
| 强腐蚀性,阴冷,密封储藏 | |
(2)若将这100毫升浓硫酸与500克水均匀混合,所得稀硫酸的质量分数是多少?
 如图是某学校实验室从化学试剂商店买回的硫酸试剂的标签上的部分内容,请阅读后计算:
如图是某学校实验室从化学试剂商店买回的硫酸试剂的标签上的部分内容,请阅读后计算: