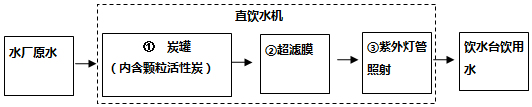
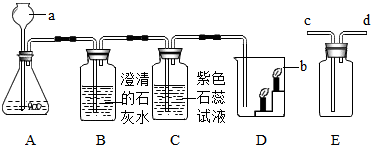
题目内容
1.观察如图所呈现的实验现象,可以得出的结论是( )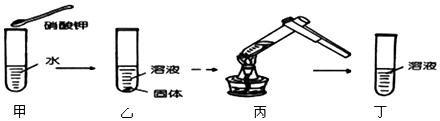
| A. | 乙图中溶液一定是饱和溶液 | |
| B. | 乙图中溶液一定是浓溶液 | |
| C. | 丁图中溶液一定是饱和溶液 | |
| D. | 丁图中溶液的溶质质量分数一定比乙图中溶液溶质质量分数小 |
分析 A、根据饱和溶液的判断方法考虑;B、溶液的浓稀与含溶质的多少有关,饱和溶液不一定是浓溶液;C、溶质全部溶解有两种情况;D、根据溶质质量分数大小与溶质和溶剂的质量有关考虑.
解答 解:A、乙图中溶液中含有不溶解的固体,所以一定是饱和溶液,故A正确;
B、溶液的浓稀与含溶质的多少有关,饱和溶液不一定是浓溶液,故B错;
C、溶质全部溶解有两种情况,可能刚好饱和,也可能不饱和,故C错;
D、丁图中溶液中溶剂的质量与乙图中溶液中溶剂的质量相等,丁图中溶解的溶质质量大,所以丁图中溶液的溶质质量分数一定比乙图中溶液溶质质量分数大,故D错.
故选A.
点评 解答本题关键是知道饱和溶液的判断方法,熟悉溶质质量分数计算方法.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
11.图2是硝酸钾的溶解度曲线.某同学在20℃时进行了如图1实验,得到相应的溶液①~⑤,下列说法正确的是( )


| A. | 保持温度不变,若在④中再加入15gKNO3固体,所得溶液仍不饱和 | |
| B. | ②③⑤中溶质的质量分数相等 | |
| C. | ②③④⑤均为饱和溶液 | |
| D. | ④→⑤可析出48.4gKNO3晶体 |
12.在电解水的实验中可以直接观察到的实验现象是( )
| A. | 水是由氢、氧两种元素组成的 | |
| B. | 每个水分子是由两个氢原子和一个氧原子构成的 | |
| C. | 在电极上均有气泡产生,两个玻璃管内气体的体积比约为2:1 | |
| D. | 有氢气和氧气产生,且体积比为2:1 |
9.某温度下,向盛有200克蔗糖溶液的烧杯中再加入10克蔗糖,充分搅拌后,一定保持不变的是( )
| A. | 溶质的质量 | B. | 溶液的质量 | C. | 溶质的质量分数 | D. | 该溶质的溶解度 |
16.下列物之间的转化,能通过一步反应实现的是( )
①CaCO3→CO2 ②CaO→Ca(OH)2 ③H2O2→H2O ④HCl→HNO3 ⑤Fe→FeCl3.
①CaCO3→CO2 ②CaO→Ca(OH)2 ③H2O2→H2O ④HCl→HNO3 ⑤Fe→FeCl3.
| A. | ①②③④ | B. | ①②③⑤ | C. | ①③④⑤ | D. | ②③④⑤ |
8.同学们在学习金属与盐溶液的反应时,老师强调:“金属K、Ca、Na必须除外”,化学兴趣小组的同学们对此产生了兴趣,并在老师的指导下,进行如下探究:
【提出问题】将金属钠没入到硫酸铜溶液中,结果会怎样?
【查找资料】
(1)少量钠通常保存在煤油中;
(2)钠是银白色的软金属,可用小刀切割,熔点97.81℃,沸点882.9℃,密度为0.97g/cm3.
【做出猜想】猜想Ⅰ:放出气体,生成蓝色沉淀,能置换出铜.
猜想Ⅱ:放出气体,生成蓝色沉淀,不能置换出铜.
【实验探究】
【现象分析】
(1)钠熔成小球是因为反应放热,温度达到钠的熔点;
(2)钠球游动,发出“嘶嘶”声响说明有气体产生;
(3)析出蓝色沉淀是因为CuSO4+2NaOH=Na2SO4+Cu(OH)2↓(用化学方程式表示).
【继续探究】有部分同学认为置换出的铜可能被蓝色沉淀掩盖,于是他们进一步探究:
【实验结论】在金属活动性顺序里,位于前面的金属(K、Ca、Na必须除外)能把位于后面的金属从它们盐的溶液里置换出来.
【提出问题】将金属钠没入到硫酸铜溶液中,结果会怎样?
【查找资料】
(1)少量钠通常保存在煤油中;
(2)钠是银白色的软金属,可用小刀切割,熔点97.81℃,沸点882.9℃,密度为0.97g/cm3.
【做出猜想】猜想Ⅰ:放出气体,生成蓝色沉淀,能置换出铜.
猜想Ⅱ:放出气体,生成蓝色沉淀,不能置换出铜.
【实验探究】
| 实验操作 | 实验现象 |
| ①取10mL一定溶质质量分数的硫酸铜溶液,倒入50mL的烧杯里 ②取一块钠,用滤纸吸干表面煤油,再切取绿豆大小的一块,投入溶液中 | 钠浮在液面上,熔化成闪亮小球,钠球游动,发出“嘶嘶”的声响,析出蓝色沉淀 |
(1)钠熔成小球是因为反应放热,温度达到钠的熔点;
(2)钠球游动,发出“嘶嘶”声响说明有气体产生;
(3)析出蓝色沉淀是因为CuSO4+2NaOH=Na2SO4+Cu(OH)2↓(用化学方程式表示).
【继续探究】有部分同学认为置换出的铜可能被蓝色沉淀掩盖,于是他们进一步探究:
| 实验操作 | 实验现象 | 结论 |
| 取烧杯中少许沉淀于试管中,再向其中加入过量的稀硫酸 | 沉淀全部溶解,溶液变蓝色 | ①反应的化学方程式为Cu(OH)2+H2SO4═CuSO4+2H2O ②沉淀中不含铜,原因是沉淀全部溶解 |
5.如图Na2CO3溶液和CaCl2溶液发生反应的“示意图”.请判断下列说法中错误的是( )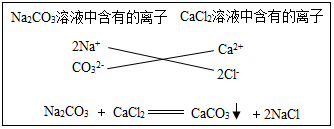

| A. | 该反应属于复分解反应 | B. | 反应前后溶液的pH值降低 | ||
| C. | 反应前后,溶液总质量保持不变 | D. | 反应能进行,是因为有沉淀生成 |